2. Уравнение состояния идеального газа
2. Уравнение состояния идеального газа
Изучение эмпирических газовых законов (Р. Бойль, Ж. Гей-Люссак) постепенно привело к представлению об идеальном газе, поскольку обнаружилось, что давление данной массы любого газа при постоянной температуре обратно пропорционально объему, занимаемому этим газом, и термические коэффициенты давления и объема с высокой точностью совпадают для различных газов, составляя, по современным данным, 1/273 град–1. Придумав способ графического представления состояния газа в координатах «давление – объем», Б. Клапейрон получил объединенный газовый закон, связывающий все три параметра:
PV = BT,
где коэффициент В зависит от вида газа и его массы.
Только через сорок лет Д. И. Менделеев придал этому уравнению более простой вид, записав его не для массы, а для единицы количества вещества, т. е. 1 кмоля.
PV = RT, (1)
где R – универсальная газовая постоянная.
Физический смысл универсальной газовой постоянной. R – работа расширения 1 кмоля идеального газа при нагревании на один градус, если давление не меняется. Для того, чтобы понять физический смысл R, представим себе, что газ находится в сосуде при постоянном давлении, и мы повысим его температуру на ?T, тогда
PV1 = RT1, (2)
и
PV2 = RT2. (3)
Вычитая из (3) уравнение (2), получим
P(V2 – V1) = R(T2 – T1).
Если правая часть уравнения равна единице, т. е. мы нагрели газ на один градус, тогда
R = P?V
Поскольку P = F/S, а ?V равно площади сосуда S, умноженной на высоту подъема его поршня ?h, имеем
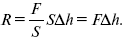
Очевидно, что справа получим выражение для работы, и это подтверждает физический смысл газовой постоянной.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
О ПУЗЫРЬКАХ ГАЗА В КРИСТАЛЛЕ
О ПУЗЫРЬКАХ ГАЗА В КРИСТАЛЛЕ Кристаллофизики часто мрачно шутят, что дефекты в кристаллах появляются всего лишь в двух случаях: когда экспериментатор, который выращивает кристаллы, хочет этого и когда он этого не хочет.Я расскажу о том, как появляются в кристаллах
ЛЕКЦИЯ № 1. Идеальный газ. Уравнение состояния реального газа
ЛЕКЦИЯ № 1. Идеальный газ. Уравнение состояния реального газа 1. Элементы молекулярно-кинетической теории Науке известно четыре вида агрегатных состояний вещества: твердое тело, жидкость, газ, плазма. Переход вещества из одного состояния в другое называют фазовым
4. Уравнение состояния реального газа
4. Уравнение состояния реального газа Исследования показали, что уравнение Менделеева – Клапейрона не очень точно выполняется при исследовании разных газов. Голландский физик Я. Д. Ван-дер-Ваальс первым понял причины этих отклонений: одна из них состоит в том, что
Получение атмосферного газа
Получение атмосферного газа После того как заработала солнечная ядерная топка, солнечный ветер (разреженная плазма большей частью из протонов и электронов, движущаяся ныне со скоростью около 400 км/ч) выдул почти весь первичный водород с гелием, а внутренние планеты
Получение или утрата атмосферного газа
Получение или утрата атмосферного газа Теперь приложим данные закономерности к внутренним планетам и посмотрим, как их первичная атмосфера приобрела нынешние очертания.Начнем с Венеры и Марса, а Землю прибережем напоследок.Венера Основное различие между нашими
Теория идеального газа
Теория идеального газа Свойства идеального газа, давшего нам определение температуры, очень просты. При постоянной температуре действует закон Бойля – Мариотта: произведение pV при изменениях объема или давления остается неизменным. При неизменном давлении сохраняется
XII. Состояния вещества
XII. Состояния вещества Железный пар и твердый воздух Не правда ли – странное сочетание слов? Однако это вовсе не чепуха: и железный пар, и твердый воздух существуют в природе, но только не при обычных условиях.О каких же условиях идет речь? Состояние вещества определяется
25. Уравнение профессора
25. Уравнение профессора В «Интерстеллар» гравитационные аномалии волнуют профессора Брэнда по двум причинам. Если он поймет их природу, это может привести к революционному скачку в наших познаниях о гравитации, к скачку столь же грандиозному, как эйнштейновская