2. Термодинамические параметры. Термодинамические показатели. Баланс напряжений
2. Термодинамические параметры. Термодинамические показатели. Баланс напряжений
Любая ТДС характеризуется параметрами: температура, давление, плотность, концентрация, мольный объем. В любой ТДС обязательно протекают процессы, и они могут быть равновесными, неравновесными, обратимыми и необратимыми.
Если в ТДС определенное свойство системы не будет изменяться во времени, т. е. оно будет одинаковым во всех точках объема, то такие процессы – равновесные.
В неравновесных процессах свойство системы будет изменяться во времени без воздействия окружающей среды.
Обратимые процессы – процессы, в которых система возвращается в первоначальное состояние.
Необратимые – когда система не возвращается в первоначальное состояние.
Функции могут зависеть от пути процесса. Функции, которые зависят от начального и конечного состояний системы и не зависят от пути процесса, – функции состояния; внутренняя энергия, энтальпия, энтропия и другие – полные дифференциалы.
Функции, которые зависят от начального и конечного состояний системы и зависят от пути процесса, не являются функциями состояния и не являются полными дифференциалами Q, A.
Функции можно разделить на две группы: экстенсивные и интенсивные.
Экстенсивное свойство системы прямо пропорционально массе системы и обладает аддитивностью (можно складывать): V, H, Uвн, S, G, F.
Интенсивное свойство системы не зависит от массы системы и не обладает свойством аддитивности: Q, A, T, P.
Давление – параметр состояния, определяемый силой, действующей в теле на единицу площади поверхности по нормали к ней. Оно характеризует взаимодействие системы с внешней средой.
Температура определяет меру интенсивности теплового движения молекул.
Значение градуса температуры и начало ее отсчета произвольны. В качестве эталона можно было бы выбрать не воду, а любое другое вещество (лишь бы его свойства однозначно изменялись с температурой, были воспроизводимы и легко поддавались измерению).
Такая произвольность исчезает, если пользоваться термодинамической (абсолютной) шкалой температур, основанной на втором законе термодинамики. Начальной точкой этой универсальной шкалы является значение предельно низкой температуры – абсолютный нуль, равный 273,15 оС.
Уравнение состояния
Уравнение, связывающее термодинамические параметры системы в равновесном состоянии, – уравнение состояния.
Вследствие взаимосвязи между свойствами системы для определения ее состояния достаточно указать лишь некоторое число свойств. Так, состояние газа можно считать заданным, если указаны два параметра, например, температура и объем, а значение третьего параметра – давления – можно определить из уравнения состояния
P = f(V, T ),
?(P, V, T ) = 0.
Графически это уравнение является уравнением поверхности, построенной на трех взаимно перпендикулярных осях, каждая из которых соответствует одному термодинамическому параметру. Таким образом, термодинамическая поверхность – геометрическое место точек, изображающих равновесные состояния системы в функциях от термодинамических параметров.
Понятие теплоты
Пусть дан изолированный сосуд, который разделен полупроницаемой перегородкой (рис. 1). В первой части сосуда температура Т1, во второй – температура Т2; Т1 > Т2.
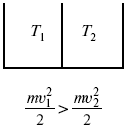
Рис. 1
Молекулы, ударяясь о полупроницаемую перегородку, будут отдавать часть энергии, а другие – принимать ее, без механического перемещения.
Форма передачи энергии от одной части системы к другой называется теплотой Q.
Мера переданной энергии от одной системы к другой – количество теплоты. Q не является функцией состояния и не является полным дифференциалом ?Q.
Понятие работы
Работа процесса – это энергия, передаваемая одним телом другому при их взаимодействии, не зависящая от температуры этих тел и не связанная с переносом вещества от одного тела к другому.
Обмен энергией между системой и внешней средой обуславливается работой, совершаемой этой системой:
А = PdV.
Работа (А) определяется суммой произведений сил, действующих на систему сил (давления и изменения объема).
Работа не является полным дифференциалом, ?А.
Если протекают равновесные процессы, то работа равновесного процесса будет максимальной величиной, по сравнению с неравновесным процессом
?Aравн > ?Aнеравн.
Если телу сообщают определенное количество теплоты, то это значит, что тело надо нагреть, а охладить систему – произвести действие, обратное нагреванию, т. е. отвести энергию.
Работа и теплота являются количественными характеристиками двух форм обмена энергией между системой и окружающей средой.
Понятие внутренней энергии
Внутренняя энергия системы Uвнскладывается из энергии поступательного и вращательного движения молекул, энергии внутримолекулярного колебательного движений атомов и атомных групп, энергии, заключающейся в ядрах атомов, энергии межмолекулярного взаимодействия.
Uвнявляется полным дифференциалом, она не зависит от пути процесса, а зависит от начального и конечного состояний системы, она однозначно непрерывна и конечна. Абсолютное значение Uвнопределить нельзя, можно определить только ее изменения.
Q и А качественно и количественно характеризуют форму передачи энергии, взаимосвязь между Q, A, Uвнустанавливает первый закон термодинамики.
Термодинамические показатели
К термодинамическим показателям относятся те, которые можно рассчитать, используя законы термодинамики, исходя из условий, что система находится в равновесии. Напряжение разложения:
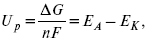
где ?G – изменение термодинамического потенциала;
п – число электронов, участвующих в химической реакции;
F– число Фарадея.
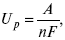
где А – максимальная работа, которую способна совершить система в равновесном состоянии.
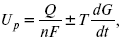
где Q – тепловой эффект реакций;
Up– термодинамическая характеристика электрохимической системы, которая мало зависит от условий электролиза.
Отклонение системы – поляризация. Электрохимическая реакция является гетерогенным процессом, и ее скорость может лимитироваться одной из стадий:
1) подвод реагирующего вещества к границе раздела фаз;
2) разряд и ионизация;
3) отвод продуктов реакции.
Поляризация, определяемая медленной стадией массопереноса – концентрационная. Если медленной стадией является стадия разряда ионизации, то поляризация называется перенапряжением. Природа и значение поляризации зависят от многих факторов: природа реагирующего вещества, материал электрода, состояние поверхности электрода, плотность тока, состав раствора и режим электролиза. Кинетический параметр – параметр, определяемый в реальных условиях электрохимической системы: ? тока, ЕАКТИВ, коэффициент диффузии, коэффициент переноса ? (на катод), ? (на анод) – доля расхода на процесс:
1) сила тока в электрохимическом аппарате J= iKSед загрузки, A, Z, iK – в зависимости от электролита;
2) скорость электролиза – образование массы вещества за единицу времени
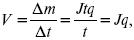
где q – электрохимический эквивалент, v электролиза – J тока,
если в 1 см2 – v – i тока.
Баланс напряжений. Напряжение на электрохимическом аппарате определяет расход электроэнергии при электролизе. Баланс напряжений на электрохимическом аппарате складывается из следующих составляющих:
UЭЛ-РЕ = Еa– Еk+ ?a+ ?k, + ?UЭЛ-ТА+ ?UДИФ+ ?UКОН+ ?UЭЛ,
где Еa– обратимый потенциал анода, В;
ЕК – обратимый потенциал катода, В;
?a– поляризация анода, В;
?k– поляризация катода, В;
?UЭЛ-ТА– падение напряжения в электролите, В;
?UДИФ– падения напряжения в диафрагме, В;
?UКОН– падение напряжения в контактах, В;
?UЭЛ – падение напряжения в электродах, В.
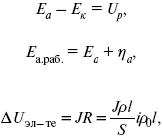
где i– плотность катодного тока;
?0 – удельное сопротивление электролита, ?0 повышается при вводе газа;
l – расстояние между электродами;
S – площадь сечения электролита;
J – электропроводность.
Коэффициент газонаполнения k = ?/?0.
Падение напряжения газозаполнения элемента определяется по формуле
?UЭЛ-ТА = il?0k.
Падение напряжения в диафрагме
?UДИФ= JRДИАФ.
Падение напряжения в контактах обычно принимают равным 5 – 10% от общего напряжения.
Падение напряжения в электродах:
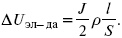
Снижение напряжения на электрохимическом аппарате – оптимальное расстояние между электродами, максимальной электропроводностью.
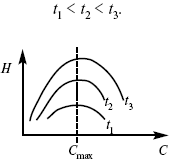
Рис. 2
К энергетическим характеристикам относятся:
1) напряжение на электрохимическом аппарате;
2) отдача по напряжению.
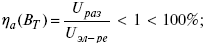
3) отдача по емкости
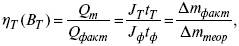
4) отдача по энергии
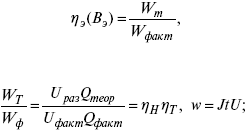
5) производительность электрохимического аппарата оценивается количеством продукта на одной затраченной энергии.
Расход электрической энергии на 1 тонну произведенного продукта определяется так:
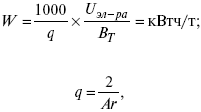
ВT – выход по току в долях единицы.
Энергетический баланс – устанавливает соотношение между видом энергии, поступающей в электролизер, и энергией, уходящей из него, демонстрируя равенство статей прихода и расхода. Электроэнергия const тока, подводимая к электролизеру, составляет:
WЭЛ= UJt.
Общее уравнение энергетического баланса имеет следующий вид:
Wэ + ?Qприхода = Wэл.хим.р-ии + Wтока + ?Qрасх,
где ?Qприхода – тепловая энергия, поступающая в электролизер с электролитом и электродами за счет вторичных процессов;
Wэл.хим.р-ии – энергия тока, затраченная на электрохимическую реакцию;
Wтока – энергия тока, перешедшая в тепловую энергию; ?Qрасх– тепловая энергия, уносимая электролитом, электродами, газами при испарении Н2О, излучении и конвекции.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
4. Термодинамические характеристики ионов в растворах электролитов
4. Термодинамические характеристики ионов в растворах электролитов ?i– химический потенциал иона. где ??изменение поверхностного потенциала данного раствора по сравнению с поверхностным потенциалом стандартного раствора;аi– «реальная» активность иона. где ln?i–
30. Физические свойства и параметры мембран
30. Физические свойства и параметры мембран Измерение подвижности молекул мембраны и диффузия частиц через мембрану свидетельствует о том, что билипидный слой ведет себя подобно жидкости. Однако мембрана есть упорядоченная структура. Эти два факта предполагают, что
ОЖИДАЕМЫЕ ПАРАМЕТРЫ КОТЛА
ОЖИДАЕМЫЕ ПАРАМЕТРЫ КОТЛА Металлическая решетка в центре котла и две другие главные решетки, образующие основную конструкцию остальной части котла, были каждая в отдельности изучены в экспоненциальных экспериментах ##18, 27 и 29. Эти эксперименты дали для коэффициента
90 Точка концентрации напряжений, или Как остановить трещину на стекле
90 Точка концентрации напряжений, или Как остановить трещину на стекле Для опыта нам потребуются: две длинные палки. Ну, раз уж начали про стекло, давайте подумаем над занятным вопросом. Часто бывает, что по стеклу начинает бежать трещина. Чаще всего это заметно на лобовых
3.11. Показатели цвета астероидов
3.11. Показатели цвета астероидов Различные приемники излучения, в том числе человеческий глаз, обладают различной чувствительностью к лучам различных длин волн. Человеческий глаз наиболее чувствителен к желтым и зеленым лучам, в то время как несенсибилизированная
4.4. Орбитальные параметры комет
4.4. Орбитальные параметры комет … Теперь известны нам Комет пути крутые, что внушали Всем ужас. Мы отныне не трепещем При появленьи бородатых звезд. Э. Галлей. «Ода Ньютону» Если орбиты большинства астероидов имеют умеренные значения эксцентриситетов и наклонов, то
Березовчук А В
Просмотр ограничен
Смотрите доступные для ознакомления главы 👉