8. Проводники первого и второго рода
8. Проводники первого и второго рода
Проводники – вещества, проводящие электрический ток благодаря наличию в них большого количества зарядов, способных свободно перемещаться (в отличие от изоляторов). Они бывают I (первого) и II (второго) рода. Электропроводность проводников I рода не сопровождается химическими процессами, она обусловлена электронами. К проводникам I рода относятся: чистые металлы, т. е. металлы без примесей, сплавы, некоторые соли, оксиды и ряд органических веществ. На электродах, выполненных из проводников I рода, происходит процесс переноса катиона металла в раствор или из раствора на поверхность металла. К проводникам II рода относятся электролиты. В них прохождение тока связано с химическими процессами и обусловлено движением положительных и отрицательных ионов.
Электроды первого рода. В случае металлических электродов первого рода такими ионами будут катионы металла, а в случае металлоидных электродов первого рода – анионы металлоида. Серебряный электрод первого рода Ag+/Ag. Ему отвечает реакция Ag+ + e- = Ag и электродный потенциал
EAg+ /Ag = Ag+ / Ag+b0lg a Ag+.
После подстановки численных значений Е 0 и b0 при 25 oС:
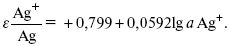
Примером металлоидных электродов первого рода может служить селеновый электрод Se2–/Se, Se + 2e- = Se2; при 25 oС ESe2–/Se0 = –0,92 – 0,03lg a Se2–.
Электроды второго рода – полуэлементы, состоящие из металла, покрытого слоем труднорастворимого соединения (соли, оксида или гидроксида) и погруженного в раствор, содержащий тот же анион, что и труднорастворимое соединение электродного металла. Схематически электрод второго рода можно представить так: АZ–/MA, M, а протекающую в нем реакцию – МА + ze = М + АZ–. Отсюда уравнением для электродного потенциала будет:
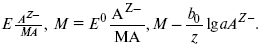
Каломельные электроды – это ртуть, покрытая пастой из каломели, и ртуть, находящаяся в контакте с раствором KCl.
Cl– / Hg2Cl2, Hg.
Электродная реакция сводится к восстановлению каломели до металлической ртути и аниона хлора:
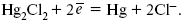
Потенциал каломельного электрода обратим по отношению к ионам хлора и определяется их активностью:
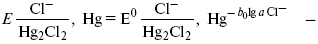
При 25 оС потенциал каломельного электрода находят по уравнению:
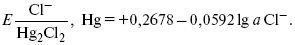
Ртутно-сульфатные электроды SO42 –/Hg2SO4, Hg аналогичны каломельным с той лишь разницей, что ртуть здесь покрыта слоем пасты из Hg и закисного сульфата ртути, а в качестве раствора используется H2SO4. Потенциал ртутно-сульфатного электрода при 25 oС выражается уравнением:
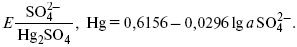
Хлорсеребряный электрод представляет собой систему Cl–/AgCl, Ag, а его потенциалу отвечает уравнение:
ECl– /AgCl, Ag = E0Cl–/AgCl, Ag –b lg aCl–
или при 25 оС:
ECl–/AgCl, Ag = 0,2224 – 0,0592 lg a Cl–.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
2. Два рода электричества
2. Два рода электричества Производя различные опыты над электричеством, люди выяснили основные его свойства. Прежде всего они открыли, что существует два рода электричества. Одно получается при натирании мехом стекла, драгоценных камней и некоторых других материалов —
5. Проводники и изоляторы
5. Проводники и изоляторы Все вещества, предметы, тела можно разделить на две группы — проводники электричества и электрические изоляторы.Чем отличаются проводники от изоляторов?Чтобы ответить на этот вопрос, сделаем следующий опыт с электроскопом. Возьмём два
Глава первая. ВЕЧНЫЙ ДВИГАТЕЛЬ ПЕРВОГО РОДА: ОТ РАННИХ ПОПЫТОК ДО «ОПЫТНЫХ ОБРАЗЦОВ»
Глава первая. ВЕЧНЫЙ ДВИГАТЕЛЬ ПЕРВОГО РОДА: ОТ РАННИХ ПОПЫТОК ДО «ОПЫТНЫХ ОБРАЗЦОВ» Мартын: Что такое perpetuum mobile? Бертольд: Perpetuum mobile, то есть вечное движение. Если найду вечное движение, то я не вижу границ творчеству человеческому… видишь ли, добрый мой Мартын: делать
Глава вторая. УТВЕРЖДЕНИЕ ЗАКОНА СОХРАНЕНИЯ ЭНЕРГИИ И КОНЕЦ ВЕЧНОГО ДВИГАТЕЛЯ ПЕРВОГО РОДА
Глава вторая. УТВЕРЖДЕНИЕ ЗАКОНА СОХРАНЕНИЯ ЭНЕРГИИ И КОНЕЦ ВЕЧНОГО ДВИГАТЕЛЯ ПЕРВОГО РОДА Пора чудес прошла, И мы теперь должны искать причины Всему, что совершается на свете. Шекспир. «Генрих
2.3. Последние вечные двигатели первого рода
2.3. Последние вечные двигатели первого рода Приведем для начала некоторые статистические данные по ppm-1, относящиеся к интересующему нас периоду. Естественно, они носят отрывочный характер, но все же достаточно показательны.По данным Британского патентного бюро за время
Глава пятая. ВЕЧНЫЕ ДВИГАТЕЛИ ВТОРОГО РОДА
Глава пятая. ВЕЧНЫЕ ДВИГАТЕЛИ ВТОРОГО РОДА Я не собираюсь критиковать. Я просто не могу понять, как может человек написать такую чепуху? Н. Бор 5.1. Какие ppm-2 изобретают теперь? Различных проектов ppm-2 предлагается очень много, и принципы их действия самые разнообразные:
Глава 3. Химия. Какого рода химические реакции подтолкнули атомы кобразованию первых живых существ?
Глава 3. Химия. Какого рода химические реакции подтолкнули атомы кобразованию первых живых существ? Сущий вздор — рассуждать сейчас о происхождении жизни; с тем же успехом можно было бы рассуждать о происхождении материи.Из письма Ч. Дарвина Дж. Д. Хукеру 29 марта