7. Метод гальваностатических кривых
7. Метод гальваностатических кривых
В этом методе анализируется зависимость Е, t при заданной i.
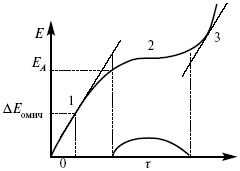
Рис. 15.1, 3 – резкое изменение потенциала, где наступает заряжение ДЭС (изменение заряда поверхности); ?E/?t– угловой коэффициент наклона, по нему можно рассчитать емкость ДЭС.
Для этого необходимо кривую записывать с помощью осцилирования, так как заряжение ДЭС происходит в течение тысячных долей секунды. В обычных условиях прибора КСП-4 кривую можно зарегистрировать с точностью до 0,1 с, определяемую по угловому коэффициенту; емкость является поляризационной емкостью (псевдоемкость). Она характеризует количество адсорбированных частиц на электроде, которые вступают в электрохимическую реакцию. Потенциал начала реакции, где первая дуга переходит во вторую – Еa. Участок 2 характеризует время протекания электрохимической реакции. Из точек пересечения касательных опускаем перпендикуляр и находим отрезок, ? – переходное время процесса, i x ? = Q– количество образовавшегося продукта. Можно на основе определения переходного времени процесса при различных плотностях тока анализировать зависимость ? от i. Для замедленной стадии диффузии, лимитирующей скорость суммарного электрохимического процесса, зависимость между переходным временем и плотностью тока:

F – число Фарадея;
С0 – объемная концентрация ионов в растворе;
D – коэффициент диффузии.
В случае замедленной диффузии
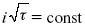
(зависит только от концентрации раствора) по угловому коэффициенту наклона прямой можно рассчитать коэффициент диффузии.

Знание зависимости переходного времени от i позволяет определить const скорости химической стадии и Кр; если электрохимическая реакция лимитируется замедленной предшествующей химической стадией то например: при катодном выделении Н2
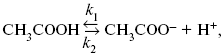
k2 – const молизации, kр = k1/k2.

? в химической стадии будет меньше ?? на величину, определяемую const скорости замедленной химической стадии.
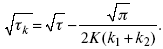
Кроме того, определение переходного времени позволяет графически находить адсорбцию веществ, участвующих в процессе. Количество электричества, определяемое длиной задержки на Е, t кривых, складывается из количества электричества, которое идет на протекание электрохимической реакции и может быть определено через долю ?, связанную с диффузией вещества к поверхности элект-рода и с адсорбцией вещества на электроде
i? = i?д+ i?адс.
При высоких плотностях тока доля электричества, которое тратится на электрохимическое превращение диффундирующих частиц, ? 0.
i? ? i?адс, i?адс = Г
где Г – величина адсорбции.
Существует несколько механизмов протекания электрохимических реакций с участием адсорбированных частиц:
1) сначала в реакцию вступают частицы, адсорбированные на поверхности электрода, а потом те, которые подходят к поверхности за счет диффузии – «сначала адсорбат»;
2) «адсорбат потом» – сначала электрохимическому превращению подвергаются диффузионные частицы, а затем те, которые адсорбируются на поверхности;
3) выполняется в тех случаях, когда поверхностная концентрация реагирующих частиц и их концентрация у поверхности подчиняется уравнению линейной изотермы адсорбции;
4) когда соотношения скоростей восстановления адсорбированных частиц и частиц диффундирующих из объема раствора, их концентрация не зависит от времени:
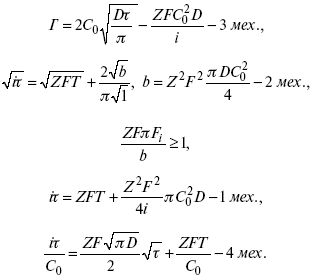

Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
II. Что такое радиоуглеродный метод датировки?
II. Что такое радиоуглеродный метод датировки? Мы говорили, что молекулы в воздухе носятся туда-сюда случайным образом и случайно выбирают, где им находиться — в гостиной Германа или в его кухне. Мы непринужденно упомянули об идее космического генератора случайных чисел,
4. Расчет KP (метод Темкина-Шварцмана)
4. Расчет KP (метод Темкина-Шварцмана) 1-й способ: термодинамический метод расчета Kp.2-й способ: Пример. Расчет Kp для реакции PbS04 распадается на РbО и S03. Результаты вычислений занесены в таблицу 2.Таблица 2Результаты
Научный метод в действии
Научный метод в действии Рассмотрим шаг за шагом классический пример работы научного метода.НаблюдениеНаблюдение. Дж. Дж. Томсон, руководитель Кавендишской лаборатории (1884–1919) в Англии, изучал поведение светового луча в электронно-лучевой трубке (прообразе современной
МЕТОД ПОДХОДА К ЗАДАЧЕ
МЕТОД ПОДХОДА К ЗАДАЧЕ 2.33. Были два пути разрешения проблемы. Один заключался в постановке ряда точных физических измерений поперечных сечений поглощения различных веществ для различных процессов, вызываемых нейтронами, и для различных энергий нейтронов. Коль скоро
ЭЛЕКТРОМАГНИТНЫЙ МЕТОД И ПРЕДЕЛЫ ЕГО ПРИМЕНИМОСТИ
ЭЛЕКТРОМАГНИТНЫЙ МЕТОД И ПРЕДЕЛЫ ЕГО ПРИМЕНИМОСТИ 9.28. Существование нерадиоактивных изотопов впервые было доказано при изучении ионизованных молекул газа, движущихся в электрическом и магнитном полях. Это — поля, которые являются основой так называемого
ФОТОГРАФИЧЕСКИЙ МЕТОД
ФОТОГРАФИЧЕСКИЙ МЕТОД Пути отдельных частиц, проходящих через вещество, можно также наблюдать в фотографической эмульсии, но длины пробега так малы, что приходится прибегать к микроскопу. На пути движения частиц образуются прямолинейные группы зерен, хорошо различимые
Резонансный метод с молекулярными пучками
Резонансный метод с молекулярными пучками Если подходящее излучение с частотой, которая точно соответствует разности между двумя энергетическими уровнями (т.е. с резонансной частотой) падает на частицу так, что заставляет ее перескочить с одного магнитного уровня на
II. Что такое радиоуглеродный метод датировки?
II. Что такое радиоуглеродный метод датировки? Мы говорили, что молекулы в воздухе носятся туда-сюда случайным образом и случайно выбирают, где им находиться – в гостиной Германа или в его кухне. Мы непринужденно упомянули об идее космического генератора случайных чисел,