ЛЕКЦИЯ V КИСЛОРОД СОДЕРЖИТСЯ В ВОЗДУХЕ. ПРИРОДА АТМОСФЕРЫ. ЕЕ СВОЙСТВА. ДРУГИЕ ПРОДУКТЫ ГОРЕНИЯ СВЕЧИ. УГЛЕКИСЛОТА, ЕЕ СВОЙСТВА
ЛЕКЦИЯ V
КИСЛОРОД СОДЕРЖИТСЯ В ВОЗДУХЕ. ПРИРОДА АТМОСФЕРЫ. ЕЕ СВОЙСТВА. ДРУГИЕ ПРОДУКТЫ ГОРЕНИЯ СВЕЧИ. УГЛЕКИСЛОТА, ЕЕ СВОЙСТВА
Мы уже убедились, что водород и кислород можно получить из воды, полученной нами при горении свечи. Вы знаете, что водород берется из свечи, а кислород, вы полагаете, берется из воздуха. Но в таком случае вы вправе спросить меня: "Почему же получается, что воздух и кислород не одинаково хорошо сжигают свечу?" Если у вас свежо в памяти, что произошло, когда я накрыл огарок банкой с кислородом, вы припомните, что тут горение шло совсем иначе, чем в воздухе. Так в чем же дело? Это очень существенный вопрос, и я приложу все старания, чтобы вы в нем разобрались; он непосредственно связан с вопросом о природе атмосферы и поэтому для нас чрезвычайно важен.
Мы располагаем несколькими способами распознавания кислорода, помимо простого сжигания в нем тех или иных веществ. Вы видели, как горит свеча в кислороде и как на воздухе; вы видели, как горит фосфор на воздухе и как в кислороде; вы видели, как горит в кислороде железо. Но, кроме этих способов распознавания кислорода, есть и другие, и я разберу некоторые из них, чтобы расширить ваш опыт и ваши знания. Вот, например, сосуд с кислородом. Я вам докажу присутствие этого газа. Я возьму тлеющую лучинку и опущу ее в кислород. Вы из прошлой беседы уже знаете, что произойдет: тлеющая лучинка, опущенная в банку, покажет вам, есть ли в ней кислород или нет. Есть! Мы это доказали горением.
А вот и другой способ распознавания кислорода, очень интересный и полезный. Здесь у меня две банки, каждая из которых наполнена газом. Они разобщены пластинкой, чтобы эти газы не смешивались. Я убираю пластинку, и начинается перемешивание газов: каждый газ как бы вползает в банку, где находится другой. "Так что же тут происходит? — спросите вы. — Они вместе не дают такого горения, какое мы наблюдали у свечи". Но вот взгляните, как присутствие кислорода можно распознать по его соединению с этим вторым веществом.[27]
Какой великолепно окрашенный газ получился. Он сигнализирует мне о присутствии кислорода. Тот же опыт можно проделать и путем смешения этого пробного газа с обыкновенным воздухом. Вот банка с воздухом — таким, в котором стала бы гореть свеча, — а вот банка с этим пробным газом. Я даю им возможность смешиваться над водой, и вот результат: содержимое испытательной банки втекает в банку с воздухом, и вы видите, что происходит точно такая же реакция. Это доказывает, что в воздухе есть кислород, т. е. то самое вещество, которое мы уже добывали из воды, полученной при сгорании свечи.
Но все-таки почему же свеча не так хорошо горит в воздухе, как в кислороде? Сейчас мы к этому перейдем. Вот у меня две банки; они наполнены газом до одинакового уровня, и на вид они одинаковы. По правде говоря, я сейчас даже не знаю, которая из этих банок содержит кислород, а которая — воздух, хотя мне известно, что их заранее наполнили именно этими газами. Но у нас есть пробный газ, и я сейчас выясню, есть ли между содержимым обеих банок какая-либо разница в способности вызывать покраснение этого газа. Я впускаю пробный газ в одну из банок. Следите, что происходит. Как видите, покраснение есть, — стало быть, здесь кислород. Испытаем теперь вторую банку. Как видите, покраснение не так отчетливо, как в первой банке.
Далее происходит любопытнейшая вещь: если смесь двух газов во второй банке хорошенько взболтать с водой, красный газ поглотится; если впустить еще порцию испытательного газа и опять взболтать банку, поглощение красного газа повторится; и так можно продолжать, пока будет оставаться кислород, без которого невозможно это явление. Если я впущу воздух, дело не изменится; но как только я введу воду, красный газ исчезнет; и я могу продолжать, таким образом, впускать все больше и больше испытательного газа, пока у меня в банке не останется нечто такое, что уже не будет окрашиваться от прибавления того вещества, которое окрашивало воздух и кислород. В чем же дело? Вы понимаете, что в воздухе, кроме кислорода, содержится еще что-то, и оно-то и остается в остатке. Сейчас я впущу в банку еще немного воздуха, и если он покраснеет, вы будете знать, что там еще оставалось какое-то количество красящего газа и что, стало быть, не его нехваткой объясняется то, что воздух израсходовался не весь.
Это поможет вам понять то, что я теперь скажу. Вы видели, что когда я сжег фосфор в банке, и получившийся из фосфора и кислорода дым осел, изрядное количество газа осталось неизрасходованным, подобно тому как наш пробный газ оставил что-то незатронутым. И действительно, после реакции остался вот этот газ, который не изменяется ни от фосфора, ни от красящего газа. Этот газ — не кислород, но, однако, это составная часть атмосферы.
Таков один способ разделения воздуха на те два вещества, из которых он состоит, т. е. на кислород, сжигающий наши свечи, фосфор и все прочее, и на вот это другое вещество — азот, в котором они не горят. Этой второй составной части в воздухе гораздо больше, чем кислорода.
Этот газ оказывается очень интересным веществом, если заняться его исследованием, но вы, может быть, скажете, что он совсем не интересный. В некоторых отношениях это так: ведь он не проявляет никаких блестящих эффектов горения. Если его испытывать зажженной лучинкой, как я испытывал кислород и водород, то он не будет ни сам гореть, как водород, ни заставлять гореть лучинку, подобно кислороду. Как бы я его ни испытывал, я не смогу от него добиться ни того, ни другого: он и не загорается и не дает гореть лучинке — он гасит горение любого вещества. При обычных условиях ничто не может в нем гореть. У него нет ни запаха, ни вкуса; это не кислота и не щелочь; по отношению ко всем нашим внешним чувствам он проявляет полное безразличие. И вы могли бы сказать: "Это ничто, оно не заслуживает внимания химии; чего ради оно существует в воздухе?"
И тут-то нам пригодится умение делать выводы из опыта. Предположим, что вместо азота или смеси азота с кислородом, наша атмосфера состояла бы из чистого кислорода, — что бы с нами сталось? Вы прекрасно знаете, что кусок железа, зажженный в банке с кислородом, сгорает дотла. При виде топящегося камина вообразите, что сталось бы с его решеткой, если бы вся атмосфера состояла из одного только кислорода: чугунная решетка стала бы гореть куда сильнее, чем каменный уголь, которым мы топим камин. Огонь в топке паровоза — это было бы все равно, что огонь на складе горючего, если бы атмосфера состояла из кислорода.
Азот разбавляет кислород, умеряет его действие и делает его полезным для нас. К тому же азот уносит с собой весь тот чад и газы, которые, как вы видели, возникают при горении свечи, рассеивает их по всей атмосфере и переносит их туда, где они оказываются нужны для поддержания жизни растений, а тем самым и человека. Таким образом, азот выполняет в высшей степени важную работу, хотя вы, ознакомившись с ним, говорите: "Ну, это совсем никчемная штука".
В своем обычном состоянии азот представляет собой неактивный элемент: никакое воздействие, кроме сильнейшего электрического разряда, да и то только в очень слабой степени, не может заставить азот непосредственно вступить в соединение с другим элементом атмосферы или с иными окружающими веществами. Это вещество совершенно индифферентное, т. е., иначе говоря, безразличное, — а тем самым и безопасное.
Но прежде чем подвести вас к этому выводу, я должен сперва кое-что рассказать вам о самой атмосфере. Вот таблица, показывающая процентный состав атмосферного воздуха:
по объему по массе
Кислород. . . . 20 22,3
Азот . . . . . 80 77,7
__________________________
100 100,0
по объему по массе Кислород 20 22,3 Азот 80 77.7 100 100Она правильно отражает относительные количества кислорода и азота в атмосфере. Отсюда мы видим, что в пяти пинтах воздуха содержится всего одна пинта кислорода на четыре пинты азота; иначе говоря, по объему азот составляет 4/5 атмосферного воздуха. Все это количество азота уходит на то, чтобы разбавить кислород и смягчить его действие; в результате и свеча надлежащим образом снабжается горючим и наши легкие могут дышать воздухом без вреда для здоровья. Ведь для нас не менее важно получать кислород для дыхания в надлежащем виде, чем иметь соответствующий состав атмосферы для горения угля в камине или свечи.
Теперь я сообщу вам массы этих газов. Пинта азота имеет массу 10 4/10 грана, а кубический фут — 1 1/6 унции. Такова масса азота. Кислород тяжелее: пинта его имеет массу 11 9/10 грана, а кубический фут — 1 1/5 унции.
Вы уже несколько раз задавали мне вопрос: "Как определяют массу газов?", и я очень рад, что этот вопрос вас заинтересовал. Сейчас я вам покажу, это дело очень простое и легкое. Вот весы, а вот медная бутылка, аккуратно выточенная на токарном станке и при всей своей прочности имеющая наименьшую возможную массу. Она совершенно непроницаема для воздуха и снабжена краном. Сейчас кран открыт, и поэтому бутылка наполнена воздухом. Весы эти очень точные, и бутылка в ее теперешнем состоянии уравновешена на них гирями на другой чашке. А вот и насос, при помощи которого мы можем нагнетать воздух в эту бутылку.
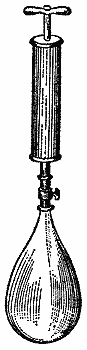
Рис. 25.
Сейчас мы накачаем в нее известное количество воздуха, объем которого будет измеряться емкостью насоса. (Накачивается двадцать таких объемов.) Теперь мы закроем кран и положим бутылку обратно на весы. Смотрите, как чашка весов опустилась: бутылка стала гораздо тяжелее, чем прежде. Емкость бутылки у нас не изменилась, — значит, воздух в том же объеме стал тяжелее. Благодаря чему? Благодаря тому воздуху, который мы в нее накачали насосом. вдобавок к имевшемуся воздуху.
Сейчас мы выпустим воздух вот в ту банку и предоставим ему возможность вернуться в прежнее состояние. Все, что мне для этого нужно сделать, сводится к тому, чтобы плотно соединить медную бутылку с банкой и открыть краны, — и вот вы видите, у нас тут собран весь тот объем воздуха, который я только что накачал в бутылку двадцатью взмахами насоса. Чтобы удостовериться, что у нас по ходу этого опыта не произошло никакой ошибки, мы опять положим бутылку на весы. Если она теперь снова окажется уравновешена первоначальной нагрузкой, мы сможем быть совершенно уверены, что мы правильно проделали опыт. Да, она уравновесилась. Вот таким образом мы и можем узнать массу тех добавочных порций воздуха, которые мы в нее накачивали. Так можно установить, что кубический фут воздуха имеет массу 1 1/5 унции.
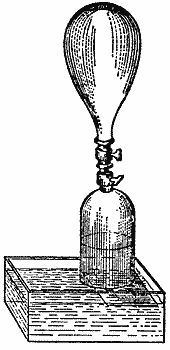
Рис. 26.
Но этот скромный опыт никак не сможет довести до вашего сознания всю сущность полученного результата. Поразительно, насколько цифры возрастают, когда мы переходим к более крупным объемам. Вот такое количество воздуха (кубический фут) имеет массу 1 1/5 унции. А как вы думаете, какова масса воздуха вон в том ящике наверху (я его специально заказывал для этих расчетов)? Воздух в нем имеет массу целый фунт. Массу воздуха в этом зале я вычислил, но эту цифру вы вряд ли угадали бы: это больше тонны. Вот как быстро возрастают массы, и вот как важно присутствие атмосферы и содержащихся в ней кислорода и азота, а также работа, которую она производит, перемещая предметы с места на место и унося вредные испарения.
Дав вам эти несколько примеров, относящихся к весомости воздуха, я перейду теперь к показу некоторых следствий из этого факта. Вам обязательно надо с ними познакомиться, иначе вам многое останется неясным. Помните ли вы такой опыт? Случалось ли вам когда-нибудь его видеть? Для него берется насос, несколько, похожий на тот, которым я только что накачивал воздух в медную бутылку.
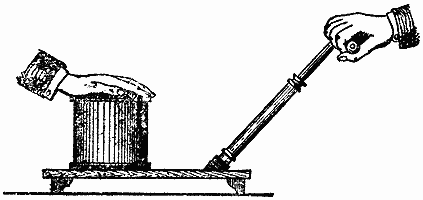
Рис. 27.
Его нужно расположить так, чтобы я мог наложить ладонь на его отверстие. В воздухе моя рука передвигается так легко, как будто она не чувствует никакого сопротивления. Как бы я ни двигался, мне почти не удается добиться такой скорости, чтобы я ощутил большое сопротивление воздуха этому движений). Но когда я кладу руку сюда (на цилиндр воздушного насоса, из которого затем выкачивается воздух), вы видите, что происходит. Почему моя ладонь пристала к этому месту так плотно, что за ней передвигается и весь насос? Смотрите! Почему мне еле-еле удается освободить руку? В чем дело? Дело в весе воздуха — того воздуха, который надо мной.
А вот и другой опыт, который, я думаю, поможет вам еще лучше разобраться в этом вопросе. Верх этой банки затянут бычьим пузырем, и когда из нее будет выкачиваться воздух, вы увидите в несколько измененном виде тот же эффект, что и в предыдущем опыте. Сейчас верх совершенно плоский, но стоит мне сделать хотя бы очень слабое движение насосом, и поглядите, как пузырь опустился, как он прогнулся внутрь. Вы сейчас увидите, как пузырь будет втягиваться все больше и больше внутрь банки, пока, наконец, он не будет окончательно вдавлен и прорван силой давящей нa него атмосферы. (Пузырь лопнул с громким хлопком.) Так вот, это произошло всецело от силы, с которой воздух давил на пузырь, и вам нетрудно будет понять, как тут обстоит дело.

Рис. 28.
Посмотрите на этот столбик из пяти кубиков: таким же образом расположены друг над другом и частицы, нагроможденные в атмосфере. Вам вполне понятно, что четыре верхних кубика покоятся на пятом, нижнем, и что если я его выну, все остальные опустятся. Так же обстоит дело и в атмосфере: верхние слои воздуха поддерживаются нижними, а когда из-под них выкачивается воздух, происходят изменения, которые вы наблюдали, когда моя ладонь лежала на цилиндре насоса и в опыте с бычьим пузырем, а сейчас увидите еще лучше.
Эту банку я завязал резиновой. перепонкой. Сейчас я буду выкачивать из нее воздух, а вы следите за резиной, отделяющей воздух внизу от воздуха наверху. Вы увидите, как будет проявляться атмосферное давление по мере выкачивания воздуха из банки. Смотрите, как втягивается резина — ведь я могу даже руку опустить в банку, — и все это только в результате мощного, колоссального воздействия воздуха над нами. Как четко проявляется здесь этот интересный факт!
После конца сегодняшней лекции вы сможете помериться силами, пытаясь разнять вот этот прибор. Он состоит из двух полых медных полушарий, плотно пригнанных друг к другу и снабженных трубкой с краном для выкачивания воздуха. Пока внутри имеется воздух, полушария легко разнимаются; однако вы убедитесь, что, когда мы выкачиваем воздух через эту трубку с краном и вы будете их тянуть — один в одну сторону, другой в другую, — никому из вас не удастся разнять полушария. Каждому квадратному дюйму площади сечения этого сосуда, когда воздух выкачан, приходится выдерживать около пятнадцати фунтов. Потом я предоставлю вам возможность испытать свои силы — попробуйте преодолеть это давление воздуха.
Вот еще интересная вещица — присоска, забава мальчиков, но только усовершенствованная для научных целей. Ведь у вас, у молодежи, полное право использовать игрушки для целей науки, тем более, что по нынешним временам из науки стали делать забаву. Вот присоска, только она не кожаная, а резиновая. Я пришлепываю ее к поверхности стола, и вы сразу видите, что она к нему прочно прилипла. А почему она так держится? Ее можно передвигать, она легко скользит с места на место, — но, как ни старайся ее поднять, она, пожалуй, скорее стол за собой потянет, чем оторвется от него. Снять ее со стола удается только тогда, когда ее сдвинешь к самому краю, чтобы впустить под нее воздух. Прижимает ее к поверхности стола только давление воздуха над ней. Вот и еще одна присоска — прижимаем их друг к другу, и вы увидите, как прочно они пристанут. Мы можем употребить их, так сказать, и по прямому назначению, т. е. прилепить к окнам и стенам, где они продержатся несколько часов и пригодятся на то, чтобы на них вешать какие-нибудь предметы.
Однако мне надо показать вам не только игрушки, но и опыты, которые вы сможете повторить дома. Наглядно доказать существование атмосферного давления можно таким изящным опытом. Вот стакан воды. Что, если я попрошу вас ухитриться так опрокинуть его вверх дном, чтобы вода при этом не пролилась? И не потому, что вы подставите руку, а исключительно благодаря атмосферному давлению.
Возьмите рюмку, налитую водой до краев или до половины, и прикройте ее какой-нибудь картонкой; опрокиньте ее и посмотрите, что произойдет с картонкой и с водой. Воздух не сможет проникнуть в рюмку, так как его не впустит вода из-за капиллярного притяжения к краям рюмки.
Я думаю, что все это даст вам правильное представление о том, что воздух — это не пустота, а нечто вещественное. Узнав от меня, что вон тот ящик вмещает фунт воздуха, а этот зал — больше тонны, вы поверите, что воздух — это не просто пустота.
Проделаем еще один опыт, чтобы убедить вас в том, что воздух действительно может оказывать сопротивление. Вы ведь знаете, какое великолепное духовое ружье можно легко устроить из гусиного пера, или трубочки, или чего-нибудь в этом роде. Взяв ломтик яблока или картофеля, надо вырезать из него маленький кусочек под размер трубки — вот так — и протолкнуть его насквозь до самого конца, как поршень. Вставив вторую пробку, мы изолируем воздух в трубке полностью. И теперь окажется, что протолкнуть вторую пробку вплотную к первой совершенно невозможно. Сжать воздух до некоторой степени можно, но если мы будем продолжать давить на вторую пробку, то она еще не успеет приблизиться к первой, как сжатый воздух вытолкнет ту из трубки, и притом с силой, напоминающей действие пороха — ведь оно тоже связано с той причиной, которую мы здесь наблюдали.
На днях я видел опыт, который мне очень понравился, так как он может быть использован, на наших занятиях. (Прежде чем к нему приступить, мне бы следовало минут пять помолчать, так как успех этого опыта зависит от моих легких.) Я надеюсь, что мне удастся силой своего дыхания, т. е. надлежащим применением воздуха, поднять яйцо, стоящее в одной рюмке, и перебросить его в другую. За успех я не ручаюсь: ведь я сейчас слишком долго говорил. (Лектор успешно проделывает опыт.) Воздух, который я выдуваю, проходит между яйцом и стенкой рюмки; под яйцом возникает напор воздуха, который оказывается в состоянии поднять тяжелый предмет: ведь для воздуха яйцо — это действительно тяжелый предмет. Во всяком случае, если вы захотите сами проделать этот опыт, лучше возьмите крутое яйцо, и тогда можно будет без риска попытаться осторожно переместить его из одной рюмки в другую силой своего дыхания.
Хотя мы изрядно долго задержались на вопросе о массе воздуха, мне хотелось бы упомянуть еще об одном его свойстве. В опыте с духовым ружьем вы убедились, что прежде чем вылетела первая картофельная пробка, мне удалось вдвинуть вторую на полдюйма или даже больше. А это зависит от замечательного свойства воздуха — от его упругости. С ней вы можете познакомиться на следующем опыте.
Возьмем оболочку, непроницаемую для воздуха, но способную растягиваться и сжиматься, а тем самым и давать нам возможность судить об упругости воздуха, содержащегося в ней. Сейчас в ней воздуха немного, и мы плотно завяжем горлышко, чтобы он не мог сообщаться с окружающим воздухом. До сих пор мы все делали так, чтобы показать давление атмосферы на поверхность предметов, а теперь, наоборот, мы избавимся от атмосферного давления. Для этого мы поместим нашу оболочку под колокол воздушного насоса, из-под которого мы будем выкачивать воздух. На ваших глазах эта оболочка расправится, надуется, как воздушный шар, и будет становиться все больше и больше, пока не заполнит собой весь колокол. Но как только я опять открою наружному воздуху доступ в колокол, наш шар сейчас же опадет. Вот вам наглядное доказательство этого удивительного свойства воздуха — его упругости, т. е. чрезвычайно большой способности сжиматься и расширяться. Это свойство имеет очень существенное значение и во многом определяет роль воздуха в природе.
Перейдем теперь к другому весьма важному разделу нашей темы. Припомните, что, когда мы занимались горением свечи, мы выяснили, что при этом образуются различные продукты горения. В числе этих продуктов — сажа, вода и еще что-то, до сих пор еще не исследованное нами. Воду мы собирали, а другим веществам предоставляли рассеиваться в воздухе. Займемся теперь исследованием некоторых из этих продуктов.
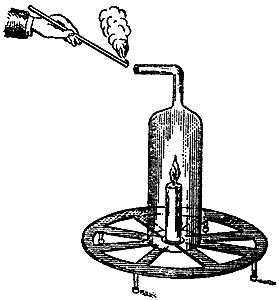
Рис. 29.
В этом деле нам поможет, в частности, следующий опыт. Вот здесь мы поставим горящую свечу и накроем ее стеклянным колпаком с отводной трубкой наверху… Свеча будет продолжать гореть, так как воздух свободно проходит внизу и наверху. Прежде всего вы видите, что колпак делается влажным; вы уже знаете, в чем тут дело: это вода, получившаяся при горении свечи от действия воздуха на водород. Но, помимо этого, что-то выходит из отводной трубки наверху; это не водяной пар, это не вода, это вещество не конденсируется, и к тому же оно отличается особенными свойствами. Вы видите, что струе, выходящей из трубки, почти удается погасить огонек, который я к нему подношу; если я буду держать зажженную лучинку прямо в выходящей струе, она совсем погаснет. "Это в порядке вещей", — скажете вы; очевидно, это потому вас не удивляет, что азот не поддерживает горения и должен гасить пламя, раз свеча в нем ни горит. Но разве тут нет ничего, кроме азота?
Здесь мне придется забежать вперед: на основе имеющихся у меня знаний я постараюсь вооружить вас научными методами исследования таких газов и выяснения этих вопросов вообще.
Возьмем пустую банку и будем держать ее над, отводной трубкой, чтобы в ней собирались продукты горения свечи. Нам нетрудно будет обнаружить, что в этой банке собрался не просто воздух, а газ, обладающий еще и другими свойствами. Для этого я беру немного негашеной извести, заливаю ее самой обыкновенной водой и хорошенько размешиваю. Вложив в воронку кружок фильтровальной бумаги, я фильтрую через нее эту смесь, и в подставленную колбу стекает чистая, прозрачная вода. Такой воды у меня сколько угодно в другом сосуде, но для убедительности я предпочитаю употреблять в дальнейших опытах именно ту известковую воду, которая приготовлена на ваших глазах.
Если налить немного этой чистой, прозрачной воды в ту банку, куда мы собрали газ, идущий от горящей свечи, вы сейчас же увидите, как произойдет перемена… Видите, вода совсем побелела! Обратите внимание, что от обыкновенного воздуха это не получится. Вот сосуд с воздухом; я в него наливаю известковой воды, но ни кислород, ни азот и ничто другое, присутствующее в этом количестве воздуха, не вызовет никаких перемен в известковой воде; как бы мы ее ни взбалтывали вместе с тем обыкновенным воздухом, который содержится в этом сосуде, она остается совершенно прозрачной. Однако если взять эту колбу с известковой водой и обеспечить ей соприкосновение со всей массой продуктов горения свечи, она быстро приобретет молочно-белый оттенок.
Это белое, похожее на мел вещество в воде, состоит из извести, которую мы взяли для приготовления известковой воды, в соединении с чем-то, появившимся из свечи, т. е. как раз с тем продуктом, который мы пытаемся уловить и о котором я сегодня буду вам рассказывать. Это вещество становится для нас видимым благодаря его реакции на известковую воду, где проявляется его отличие от кислорода, азота, от водяного пара; это — новое для нас вещество, получаемое из свечи. Поэтому, чтобы как следует разобраться в горении свечи, нам следует еще узнать, как и из чего получается этот белый порошок. Можно доказать, что это действительно мел; если положить в реторту влажный мел и раскалить его докрасна, из него выделится как раз то самое вещество, что и из горящей свечи.
Существует и другой, лучший способ получения этого вещества, и притом в больших количествах, если хотят выяснить, каковы его основные свойства. Это вещество, оказывается, в изобилии есть там, где вам не пришло бы в голову подозревать его присутствие. Этот газ, выделяющийся при горении свечи и называемый углекислым газом, в огромных количествах содержится во всех известняках, в мелу, в раковинах, в кораллах. Это интересная составная часть воздуха находится в связанном виде во всех этих камнях; обнаружив это вещество в таких горных породах, как мрамор, мел и т. п., химик д-р Блэк[28] назвал его "связанным воздухом", так как оно находится уже не в газообразном состоянии, а вошло в состав твердого тела.
Этот газ легко получить из мрамора. На дне вот этой банки немного соляной кислоты; горящая лучинка, опущенная в банку, покажет, что в ней до самого дна нет ничего, кроме обыкновенного воздуха. Вот кусочки мрамора — прекрасного высокосортного мрамора; я их бросаю в банку с кислотой и получается нечто вроде бурного кипения. Однако выделяется при этом не водяной пар, а какой-то газ; и если я сейчас испытаю содержимое банки горящей лучинкой, я получу точно такой же результат, как от газа, выходившего из отводной трубки над горящей свечой. Не только действие здесь то же самое, но и вызвано оно точно таким же веществом, какое выделялось из свечи; этим способом мы можем получать углекислый газ в больших количествах: ведь сейчас наша банка уже почти наполнилась.
Мы можем также убедиться, что этот газ содержится не только в мраморе.
Вот большая банка с водой, в которую я насыпал мелу (такого сорта, какой можно найти в продаже для штукатурных работ, т. е. промытого в воде и очищенного от грубых частиц).
Вот крепкая серная кислота; именно эта кислота нам потребуется, если вы дома захотите повторить наши опыты (обратите внимание на то, что при действии этой кислоты на известняк и подобные породы получается нерастворимый осадок, тогда как соляная кислота дает вещество растворимое, от которого вода так не густеет).
Вас может заинтересовать вопрос, почему я проделываю этот опыт в такой посуде. Для того чтобы вы могли повторить в небольшом масштабе то, что я здесь делаю в крупном. Здесь вы увидите то же явление, что и раньше: в этой большой банке я добываю углекислый газ, по своей природе и свойствам одинаковый с тем, который получался у нас при горении свечи в атмосферном воздухе. И как бы ни различались между собой эти два способа получения углекислого газа, вы к концу нашего исследования убедитесь, что он оказывается во всех отношениях одинаков, независимо от способа получения.
Перейдем к следующему опыту для выяснения природы этого газа. Вот здесь полная банка этого газа — испытаем его горением, т. е. так, как мы уже испытывали целый ряд других газов. Как видите, он и сам не горит и не поддерживает горения. Далее, растворимость его в воде незначительна: ведь, как вы видели, его легко собирать над водой. Кроме того, вы знаете, что он дает характерную реакцию с известковой водой, которая от него белеет; и наконец, углекислый газ входит как одна из составных частей в углекислую известь, т. е. известняк.
Теперь я покажу вам, что углекислый газ все-таки растворяется в воде, хоть и незначительно, и в этом отношении, стало быть, отличается от кислорода и водорода. Вот прибор для получения такого раствора. В нижней части этого прибора находятся мрамор и кислота, а в верхней — холодная вода. Клапаны устроены так, чтобы газ мог проходить из нижней части сосуда в верхнюю. Сейчас я пущу мой аппарат в действие… Видите, как сквозь воду поднимаются пузырьки газа. Аппарат работал у нас со вчерашнего вечера, и мы, несомненно, обнаружим, что сколько-нибудь газа уже успело раствориться. Я открываю кран, отливаю этой воды в стакан и пробую ее на вкус. Да, она кисловатая — в ней есть углекислота. Если ее слить с известковой водой, получится характерное побеление, доказывающее присутствие углекислоты.
Углекислый газ — очень тяжелый, он тяжелее атмосферного воздуха. В таблице приводятся массы углекислого газа и некоторых других газов, которые мы с вами исследовали.
Пинта Кубич. фут
(граны) (унции)
Водород . . . . 3/4 1/12
Кислород . . . . 11 9/10 1 1/3
Азот . . . . . . 10 4/10 1 1/6
Воздух . . . . . 10 7/10 1 1/5
Углекислый газ . 16 1/3 1 9/10
Пинта Кубич. фут (граны) (унции) Водород 3/4 1/12 Кислород 11 9/10 1 1/3 Азот 10 4/10 1 1/6 Воздух 10 7/10 1 1/5 Углекислый газ 16 1/3 1 9/10Тяжесть углекислого газа можно показать на целом ряде опытов. Прежде всего возьмем, например, высокий стакан, в котором нет ничего, кроме воздуха, и попытаемся налить в него немного углекислого газа из этого сосуда. По виду нельзя судить, удалось ли мне это или нет; но у нас есть способ проверки (опускает в стакан горящую свечку, она гаснет). Вот видите, газ действительно перелился сюда. И если бы я испытал его известковой водой, это испытание дало бы тот же результат. У нас получился как бы колодец с углекислым газом на дне (к сожалению, с такими колодцами иногда приходится иметь дело в действительности); опустим в него вот это миниатюрное ведерко. Если на дне сосуда есть углекислый газ, его можно зачерпнуть этим ведерком и извлечь из "колодца". Сделаем проверку лучинкой… Да, смотрите, ведерко полно углекислого газа.

Рис. 30.
Вот еще один опыт, показывающий, что углекислый газ тяжелее воздуха. На весах уравновешена банка; сейчас в ней только воздух. Когда я в нее наливаю углекислый газ, она сразу же опускается от веса газа. Если я исследую банку горящей лучинкой, вы убедитесь, что туда действительно попал углекислый газ: содержимое банки не может поддерживать горение.
Рис. 31.
Если я надую мыльный пузырь своим дыханием, т. е., конечно, воздухом, и сброшу его в эту банку с углекислым газом, он не упадет на дно. Но сперва я возьму вот такой шарик, надутый воздухом, и при его посредстве проверю, где приблизительно приходится уровень углекислого газа в этой банке. Вот видите, шарик не падает на дно; я подливаю в банку углекислого газа, и шарик поднимается выше. Теперь посмотрим, удастся ли мне, надув мыльный пузырь, заставить его таким же образов держаться во взвешенном состоянии. (Лектор надувает мыльный пузырь и сбрасывает его в банку в углекислым газом, где пузырь и остается во взвешенном состоянии.) Видите, мыльный пузырь, как и воздушный шарик, держится на поверхности углекислого газа именно потому, что этот газ тяжелее воздуха,
Итак, вы ознакомились, во-первых, с тем, что при горении свечи получается углекислый газ, и, во-вторых, с его физическими свойствами и массой. В следующий раз я покажу вам, из чего он состоит и откуда берутся его составные части.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
Познать физические свойства — значит научиться измерять
Познать физические свойства — значит научиться измерять Попробуйте при случае подсчитать, сколько цветов в радуге. Эту задачу выполнить невозможно. Между полосами красной и оранжевой, синей и голубой, как и между любыми соседними полосами, нет резких границ, между ними
Волновые свойства света. Опыт Юнга
Волновые свойства света. Опыт Юнга Ньютоновская корпускулярная гипотеза света господствовала очень долго — более полутораста лет. Но вот в начале XIX века английский физик Томас Юнг (1773—1829) и французский физик Огюстен Френель (1788—1827) произвели такие опыты, которые
Свет и химические свойства атомов
Свет и химические свойства атомов С оптическими спектрами атомов мы имеем дело с первых страниц нашей книжки. Это их наблюдали физики на заре развития спектрального анализа. Это они служили приметами для опознавания химических элементов, ибо у каждого химического
ЛЕКЦИЯ II СВЕЧА. ЯРКОСТЬ ПЛАМЕНИ. ДЛЯ ГОРЕНИЯ НЕОБХОДИМ ВОЗДУХ. ОБРАЗОВАНИЕ ВОДЫ
ЛЕКЦИЯ II СВЕЧА. ЯРКОСТЬ ПЛАМЕНИ. ДЛЯ ГОРЕНИЯ НЕОБХОДИМ ВОЗДУХ. ОБРАЗОВАНИЕ ВОДЫ На прошлой лекции мы рассмотрели общие свойства и расположение жидкой части свечи, а также и то, каким образом эта жидкость попадает туда, где происходит горение. Вы убедились, что когда свеча
ЛЕКЦИЯ III ПРОДУКТЫ ГОРЕНИЯ. ВОДА, ОБРАЗУЮЩАЯСЯ ПРИ ГОРЕНИИ. ПРИРОДА ВОДЫ. СЛОЖНОЕ ВЕЩЕСТВО. ВОДОРОД
ЛЕКЦИЯ III ПРОДУКТЫ ГОРЕНИЯ. ВОДА, ОБРАЗУЮЩАЯСЯ ПРИ ГОРЕНИИ. ПРИРОДА ВОДЫ. СЛОЖНОЕ ВЕЩЕСТВО. ВОДОРОД Надеюсь, вы хорошо помните, что в конце прошлой лекции я использовал выражение "продукты горения свечи". Ведь мы убедились, что когда горит свеча, мы можем при помощи
ЛЕКЦИЯ IV ВОДОРОД В СВЕЧЕ. ВОДОРОД СГОРАЕТ И ПРЕВРАЩАЕТСЯ В ВОДУ. ДРУГАЯ СОСТАВНАЯ ЧАСТЬ ВОДЫ — КИСЛОРОД
ЛЕКЦИЯ IV ВОДОРОД В СВЕЧЕ. ВОДОРОД СГОРАЕТ И ПРЕВРАЩАЕТСЯ В ВОДУ. ДРУГАЯ СОСТАВНАЯ ЧАСТЬ ВОДЫ — КИСЛОРОД Я вижу, вам еще не надоела свеча, иначе вы бы не стали проявлять столько интереса к этой теме. Когда наша свеча горела, мы убедились, что она дает в точности такую же воду,
ЛЕКЦИЯ VI УГЛЕРОД, ИЛИ УГОЛЬ. СВЕТИЛЬНЫЙ ГАЗ. ДЫХАНИЕ И ЕГО СХОДСТВО С ГОРЕНИЕМ СВЕЧИ. ЗАКЛЮЧЕНИЕ
ЛЕКЦИЯ VI УГЛЕРОД, ИЛИ УГОЛЬ. СВЕТИЛЬНЫЙ ГАЗ. ДЫХАНИЕ И ЕГО СХОДСТВО С ГОРЕНИЕМ СВЕЧИ. ЗАКЛЮЧЕНИЕ Одна дама, оказывающая мне честь посещением этих лекций, сделала мне еще и то одолжение, что любезно прислала мне вот эти две свечи, привезенные из Японии. Как видите, они еще
20. Механические свойства твердых тел и биологических тканей
20. Механические свойства твердых тел и биологических тканей Характерным признаком твердого тела является способность сохранять форму. Твердые тела можно разделить на кристаллические и аморфные.Отличительным признаком кристаллического состояния служит анизотропия –
21. Механические свойства биологических тканей
21. Механические свойства биологических тканей Под механическими свойствами биологических тканей понимают две их разновидности. Одна связана с процессами биологической подвижности: сокращение мышц животных, рост клеток, движение хромосом в клетках при их делении и др.
30. Физические свойства и параметры мембран
30. Физические свойства и параметры мембран Измерение подвижности молекул мембраны и диффузия частиц через мембрану свидетельствует о том, что билипидный слой ведет себя подобно жидкости. Однако мембрана есть упорядоченная структура. Эти два факта предполагают, что
38. Напряженность магнитного поля и другие его свойства
38. Напряженность магнитного поля и другие его свойства Напряженность магнитного поля зависит от свойства среды, а определяется только силой тока, протекающего по контуру. Напряженность магнитного поля, созданного постоянным током, слагается из напряженности полей,
39. Свойства магнетиков и магнитные свойства тканей человека
39. Свойства магнетиков и магнитные свойства тканей человека Молекулы парамагнетиков имеют отличные от нуля магнитные моменты. При отсутствии магнитного поля эти моменты расположены хаотически и их намагниченность равна нулю. Степень упорядоченности магнитных