5. Расчет равновесного состава химического равновесия
5. Расчет равновесного состава химического равновесия
Равновесный состав можно рассчитать только для газовой системы
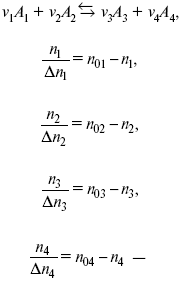
равновесная концентрация.
Исходная концентрация всех компонентов

Изменение каждого компонента по числу молей (или стехиометрическому коэффициенту):
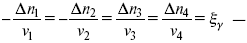
??– (пробег реакции) – химическая переменная.
Она показывает изменение количества вещества по числу молей. Если реакция не началась, то ?? = 0. Если количество исходных веществ превратилось в такое же количество продуктов реакции, то ?? = 1.
3H2 + N2 = 2NH3; ??= 1,
1,5H2 + 0,5N2 = NH3; ??= 0,5,
v1 А 1 + v2А2 = v3А3+ v4А4, – газовая реакция.
Рассчитать равновесный состав по третьему компоненту при условии, что А = а моль/л; В = в моль/л.
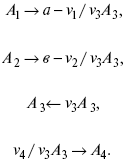
Рассчитываем по 4 компоненту:
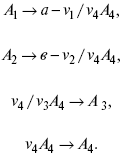
Задача.
Газообразные вещества реагируют по уравнению:
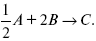
Общее давление в газовой смеси – Робщ, общий объем – Vоб . Рассчитать KP и Kс.
Найти парциальное давление каждого компонента.
Вещества А и В превращаются в С в количестве Х. Исходные вещества А= 2 моль, В= 1 моль.
Для того, чтобы найти парциальное давление, мы должны Роб умножить на мольную долю. Мольная доля определяется отношением числа молей каждого компонента, отнесенного к общему числу молей всех компонентов.
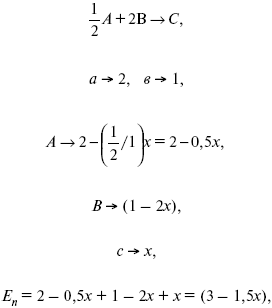
где En – общее число молей, участвующих в этой газовой смеси.
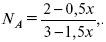
где NA – мольная доля А.
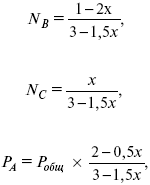
где РА – парциальное давление.

Расчет Kc:
?v= l – 0,5 – 2 = – 1,5,
где ?v– изменение количества молей.
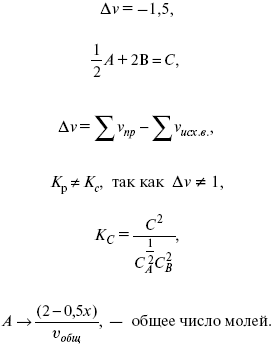
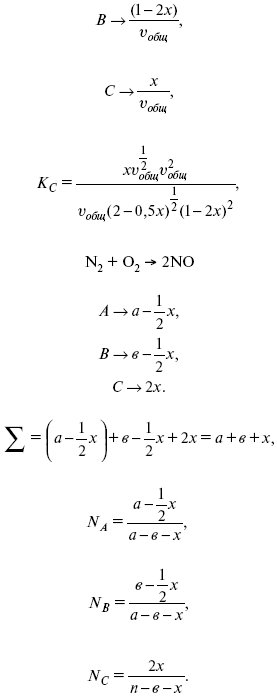
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
ФИГУРЫ РАВНОВЕСИЯ ВРАЩАЮЩЕЙСЯ ЖИДКОСТИ
ФИГУРЫ РАВНОВЕСИЯ ВРАЩАЮЩЕЙСЯ ЖИДКОСТИ Вкратце остановимся на проблеме фигур равновесия вращающейся жидкости, в разработку которой основной вклад внес А.М. Ляпунов.Ньютон показал, что под влиянием центробежных сил и взаимного притяжения своих частиц однородная
1. Понятие химического равновесия. Закон действующих масс
1. Понятие химического равновесия. Закон действующих масс При протекании химической реакции через некоторое время устанавливается химическое равновесие. Существует два признака химического равновесия: кинетический, термодинамический. В кинетическом – ?пр = ?обр, в
4. Расчет KP (метод Темкина-Шварцмана)
4. Расчет KP (метод Темкина-Шварцмана) 1-й способ: термодинамический метод расчета Kp.2-й способ: Пример. Расчет Kp для реакции PbS04 распадается на РbО и S03. Результаты вычислений занесены в таблицу 2.Таблица 2Результаты
1. Суть физико-химического анализа
1. Суть физико-химического анализа Задача физико-химического анализа состоит в установлении зависимости свойств равновесной системы от параметров состояния. Под параметрами состояния обычно понимают: состав, давление, температуру. Зависимости выражаются в виде
3. Физико-химические методы анализа состава сплавов
3. Физико-химические методы анализа состава сплавов Различают термический и рентгеноструктурный анализ.Физико-химический анализ – область химии, изучающая посредством сочетания физических и геометрических методов превращения, происходящие в равновесных
5. Исследование явления высокотемпературной сверхпроводимости в оксидах сложного состава
5. Исследование явления высокотемпературной сверхпроводимости в оксидах сложного состава В настоящее время наиболее изучены оксиды на основе Cu и Bi, в состав оксидов, помимо Cu, Bi, входят щелочно-земельные металлы – B a, C a, Sr, р.з.м. (редкоземельные) – лантаниды, Ir, известны
Глава 6 Звезда — газовый шар, находящийся в состоянии равновесия
Глава 6 Звезда — газовый шар, находящийся в состоянии равновесия Представляется почти очевидным тот факт, что подавляющее большинство звезд не меняет своих свойств в течение огромных промежутков времени. Это утверждение совершенно очевидно для интервала времени по
РАСЧЕТ РИСКОВ
РАСЧЕТ РИСКОВ В идеале одним из первых шагов должен быть расчет рисков. Иногда мы, люди, просто неверно оцениваем вероятности. Когда журналист Джон Оливер расспрашивал Уолтера Вагнера, одного из истцов в деле против БАКа, о черных дырах, то Вагнер полностью потерял
ВЫБОР ПРОЦЕССА ХИМИЧЕСКОГО РАЗДЕЛЕНИЯ
ВЫБОР ПРОЦЕССА ХИМИЧЕСКОГО РАЗДЕЛЕНИЯ 8.20. Задача заключается в химическом выделении плутония с дневной производительностью, скажем, в несколько граммов из нескольких тысяч граммов урана, загрязненного большими количествами опасно радиоактивных продуктов деления,