РАДИОАКТИВНОСТЬ И СТРОЕНИЕ АТОМА
РАДИОАКТИВНОСТЬ И СТРОЕНИЕ АТОМА
1.6. Явления радиоактивности, открытые А. Беккерелем в 1896 г. и вслед затем изучавшиеся Пьером и Марией Кюри, Э. Резерфордом и многими другими, сыграли ведущую роль в открытии общих законов строения атома и в подтверждении эквивалентности массы и энергии.
ИОНИЗАЦИЯ РАДИОАКТИВНЫМИ ВЕЩЕСТВАМИ
1.7. Первым из наблюдавшихся явлений радиоактивности было явление почернения фотографической пластинки под действием минералов, содержащих уран. Хотя до некоторой степени еще и сейчас пользуются этим свойством при исследовании радиоактивности, наибольшее научное значение имеет способность радиоактивных веществ ионизовать газы. Воздух и другие газы в нормальных условиях не проводят электричества иначе невозможно было бы эксплоатировать линии электропередачи и электрические машины на открытом воздухе. Однако, при некоторых условиях молекулы воздуха распадаются на положительно и отрицательно заряженные частицы, называемые ионами. Ионизованный таким образом воздух становится проводником электричества. Через несколько месяцев после первого открытия радиоактивности Беккерель обнаружил способность урана ионизовать воздух. В частности, он нашел, что заряд электроскопа очень быстро исчезает, вследствие ионизации воздуха, если вблизи электроскопа поместить какую-нибудь из солей урана. (То же самое произойдет с зарядом аккумулятора, если близко к нему поднести достаточное количество радиоактивного вещества). С того времени скорость разрядки электроскопа всегда служит мерой интенсивности радиоактивности. Более того, почти все современные приборы для изучения явлений радиоактивности прямо или косвенно основаны на ионизационном эффекте. Элементарное описание подобных приборов электроскопов, счетчиков Гейгера-Мюллера, ионизационных камер и камер Вильсона приведено в Приложении 1.
РАЗЛИЧНЫЕ ИЗЛУЧЕНИЯ И ЧАСТИЦЫ
1.8. На различия в природе «излучений» указывает тот факт, что ионизующая способность разных радиоактивных веществ различна как по своему характеру, так и по интенсивности. Некоторые излучения обладают значительно большей проникающей способностью. чем другие; следовательно, два радиоактивные образца, оказывающие одинаковое действие на неэкранированный электроскоп, могут совершенно по разному действовать на электроскоп, если он экранирован, т. е. если между электроскопом и образцом помещены экраны.
1.9. Изучение поглощения и других явлений показало, что радиоактивные вещества испускают три типа «излучений»: ?-частицы, являющиеся очень быстрыми ионизованными атомами гелия (ядрами атомов гелия), ?-частицы, являющиеся очень быстро движущимися электронами, и ?-лучи, представляющие собою электромагнитное излучение, подобное рентгеновским лучам. Из всех этих излучений лишь ?-лучи правильно называть излучением, но даже они со своему действию весьма напоминают частицы, благодаря своей малой длине волны. Такая «частица», или квант ?-излучения, называется фотоном, ?-лучи обладают весьма большой проникающей способностью, ?- и ?-лучи меньшей. Но даже несмотря на то, что ?- и ?-лучи обладают не очень большой проникающей способностью, кинетическая энергия их для частиц атомных размеров огромна она в тысячи раз превосходит кинетическую энергию газовых молекул, которую они имеют благодаря тепловому движению, и в тысячи раз больше, чем изменения энергии на один атом в химических реакциях. Именно по этой причине Эйнштейн предположил, что изучение радиоактивности сможет доказать эквивалентность массы и энергии.
АТОМ
1.10. Прежде чем рассматривать вопрос о том, какие атомы испускают ?-, ?- и ?-лучи, и обсуждать законы, управляющие этим испусканием, мы изложим общепринятые представления о строении атомов, частично основанные на изучении радиоактивности.
1.11. Согласно нашим современным взглядам, каждый атом состоит из небольшого тяжелого ядра с диаметром, примерно в 10-12 см, окруженного большой пустой областью с диаметром 10-8 см, в которой, в некоторой степени подобно планетам вокруг солнца, движутся электроны. Ядро несет целое число положительных зарядов, каждый из которых равен 1.610-19 кулонов. (Единицы см. в Приложении 2). Каждый электрон несет один отрицательный заряд такой же величины, а число электронов, обращающихся вокруг ядра, равно числу положительных зарядов ядра, так что заряд атома в целом равен нулю.
1.12. Атомный номер и электронная структура. Число положительных зарядов ядра называется атомным номером X. Он определяет число электронов во внеядерной структуре атома, которое, в свою очередь, определяет его химические свойства. Таким образом все атомы данного химического элемента имеют один и тот же атомный номер, и обратно, все атомы, имеющие одинаковые атомные номера, являются атомами одного и того же элемента, независимо от возможных различий в строении их ядер. Внеядерные электроны атома располагаются последовательными оболочками, согласно твердо установленным законам. Оптические спектры возникают вследствие возмущений в наружных частях этой электронной структуры; рентгеновские лучи возникают в результате возмущений электронов оболочек, близких к ядру. Химические свойства атома зависят от наиболее удаленных от ядра электронов, и образование химических соединений сопровождается незначительными перегруппировками этих электронных структур. Отсюда следует, что когда при окислении, горении, взрыве или каком-либо другом химическом процессе выделяется энергия, она выделяется за счет этих структур, так что группировка электронов в атомах, образовавшихся в результате реакции, должна иметь меньшую энергию. (Предполагают, что общая масса этих продуктов соответственно меньше, но обнаружить это пока невозможно). Атомные ядра не испытывают изменений при обычных химических реакциях.
1.13. Массовое число. Не только положительный заряд ядра всегда выражается целым числом, равным числу электронных зарядов, но и масса ядра всегда приближенно равна целому кратному основной единицы массы, почти равной массе протона ядра атома водорода (см. Приложение 2). Это целое число называют массовым числом А; оно всегда по меньшей мере вдвое больше атомного номера; исключение составляет водород и редкий изотоп гелия. Так как масса протона примерно в 1800 раз больше массы электрона, то масса ядра почти равна массе всего атома.
1.14. Изотопы и изобары. Атомы, имеющие один и тот же атомный номер, но разные массовые числа, называются изотопами. Химически они тождественны, будучи лишь разновидностями одного и того же химического элемента. Атомы, имеющие одинаковые массовые числа, но разные атомные номера, называются изобарами и представляют собою различные химические элементы.
РАДИОАКТИВНОСТЬ И ЯДЕРНЫЕ ПРЕВРАЩЕНИЯ
1.15. Если атом испускает ?-частицу (которая имеет атомный номер два и массовое число четыре), то он становится атомом уже другого элемента, атомный номер которого меньше на две, а массовое число на четыре единицы. При испускании ядром ?-частицы атомный номер на единицу возрастает, а массовое число остается неизменным. В некоторых случаях эти изменения сопровождаются испусканием ?-лучей. Элементы, которые самопроизвольно изменяются или «распадаются» указанным образом неустойчивы и их принято называть «радиоактивными». Это свойство испускать ?- или ?-частицы обнаруживают только те естественные элементы (за редкими исключениями), которые имеют очень большие атомные номера и массовые числа, например, уран, торий, радий и актиний, т. е. элементы с самым сложным строением ядер.
ПЕРИОД ПОЛУРАСПАДА; РАДИОАКТИВНЫЕ ЯДРА
1.16. Все атомы данного радиоактивного изотопа обладают одинаковой вероятностью распада в заданный промежуток времени, так что достаточно большой образец радиоактивного вещества, содержащий многие миллионы атомов, всегда превращается или «распадается» с одной и той же скоростью. Эта скорость, с которой вещество меняется или «распадается», выражается через «период полураспада» время, необходимое для распада половины всего первоначального количества атомов; это время, очевидно, постоянно для каждой данной разновидности атомов. Периоды полураспада (или просто периоды) радиоактивных веществ лежат в интервале от долей секунды для самых неустойчивых из них до миллиардов лет для тех веществ, которые лишь слегка неустойчивы. Часто «дочернее» ядро, подобно своему радиоактивному «родителю», само является радиоактивным и распадается и т. д., пока через несколько последующих поколений ядер не образуется устойчивое ядро. Существуют три такие семейства или ряда, включающие в общей сложности около сорока разных радиоактивных веществ (рис. 1). Ряд радия начинается с одного изотопа урана, ряд актиния с другого изотопа урана и ряд тория начинается с тория. Конечными продуктами каждого ряда, образующимися после десяти или двенадцати последовательных испусканий ?- и ?-частиц, являются устойчивые изотопы свинца.
ПЕРВЫЕ ОПЫТЫ ИСКУССТВЕННОГО РАСЩЕПЛЕНИЯ ЯДРА
1.17. До 1919 года никому не удавалось нарушить устойчивость обычных ядер или повлиять на скорости распада радиоактивных ядер. В 1919 г. Резерфорд показал, что ?-частицы, обладающие большой энергией, способны вызвать изменения в ядре обычного
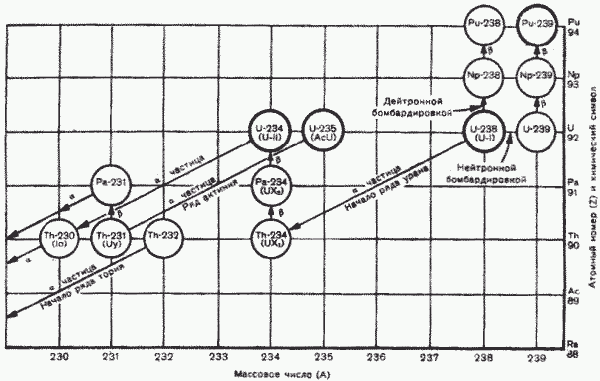
Рис. 1. Начальные участки трех естественных рядов и новые трансурановые элементы нептуний и плутоний.
элемента. В частности, ему удалось превратить несколько атомов азота, бомбардируя их ?-частицами, в атомы кислорода. Процесс можно представить в таком виде:
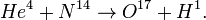
Это символическое равенство означает, что ядро гелия с массовым числом 4 (?-частица), сталкиваясь с ядром азота, имеющим массовое число 14, дает ядро кислорода с массовым числом 17 и ядро водорода с массовым числом 1. Ядро водорода, называемое Протоном, играет особенно важную роль, так как из всех ядер оно обладает наименьшей массой. Хотя в естественных радиоактивных процессах протоны не обнаруживаются, имеется много прямых указаний на то, что они могут быть выбиты из ядер.
НЕЙТРОН
1.18. В течение десятилетия, последовавшего за работами Резерфорда, было произведено много аналогичных экспериментов с подобными же результатами. Один ряд экспериментов этого типа привел к открытию нейтрона частицы, свойства которой будут рассмотрены подробнее, так как именно она является основой в осуществлении всего проекта.
1.19. В 1930 г. В. Боте и Г. Беккер в Германии нашли, что когда очень быстрые естественные ?-частицы из полония попадали на легкие элементы бериллий, бор и литий, то последние испускали излучение необычайно большой проникающей способности. Сперва это излучение было принято за ?-излучение, хотя оно было более проникающим, чем все известные ?-лучи, и объяснить с этой точки зрения детали результатов опыта было весьма трудно. Следующий важный шаг был сделан в 1932 г. в Париже Ирен Кюри и Ф. Жолио. Они показали, что если это неизвестное излучение попадает на парафин или на какое-нибудь другое соединение. содержащее водород, то это вещество выбрасывает протоны, обладающие очень большой энергией. Появление быстрых протонов само по себе не противоречило предположению, что новое излучение по своей природе состоит из ?-лучей, но эту гипотезу оказывалось все труднее и труднее примирить с детальным количественным анализом экспериментальных данных. Наконец (позднее, в 1932 г.), Дж. Чэдвик в Англии произвел ряд опытов, показавших, что гипотеза ?-лучей несостоятельна. Он предположил, что в действительности новое излучение состоит из незаряженных частиц, масса которых приблизительно равна массе протона, и это предположение подтвердил рядом опытов. Такие незаряженные частицы называются теперь нейтронами.
1.20. Одной из особенностей нейтронов, отличающих их от других субатомных частиц, является отсутствие у них заряда. Это свойство нейтронов, задержавшее их открытие, делает невозможным их непосредственное наблюдение и придает им большую проникающую способность. Благодаря отсутствию заряда нейтроны являются важными агентами в ядерных превращениях. Атом, разумеется, в своем нормальном состоянии также незаряжен, но он в десять тысяч раз больше нейтрона и состоит из сложной системы отрицательно заряженных электронов, расположенных на больших расстояниях вокруг положительно заряженного ядра. Заряженные частицы, например, протоны, электроны или ?-частицы, и электромагнитные излучения (например, ?-лучи), проходя через вещество, теряют энергию. При этом возникают электрические взаимодействия, сопровождающиеся ионизацией атомов вещества. (Именно благодаря такому процессу ионизации воздух становится электропроводным на пути электрических искр или вспышек молнии). Энергия, затраченная на ионизацию, равна энергии, потерянной заряженными частицами, которые при этом замедляются, или ?-лучами, которые при этом поглощаются. Однако, такие силы действовать на нейтрон не могут; на него может оказывать влияние лишь сила очень близкого действия, т. е. сила, проявляющая себя только тогда, когда нейтрон подходит к атомному ядру на очень малое расстояние. Это те же силы, которые удерживают вместе составные части ядра, несмотря на силы взаимного отталкивания положительных зарядов внутри него.
Свободный нейтрон движется беспрепятственно до тех пор, пока он не испытает «лобового» столкновения с атомным ядром. Так как ядра очень малы, то такие столкновения происходят довольно редко, и до столкновения нейтрон проходит длинный путь. В случае столкновения «упругого» типа обычный закон сохранения количества движения применяется таким же образом, как и в случае упругого удара биллиардных шаров. Если масса ядра, воспринявшего удар, велика, то оно приобретает относительно малую скорость; но если удар воспринят протоном, масса которого приблизительно равна массе нейтрона, то протон полетит вперед, получив значительную часть начальной скорости нейтрона, который сам соответственно замедлится. Можно обнаружить при этом атомы отдачи, образовавшиеся в результате этих столкновений, так как они заряжены и вызывают ионизацию.
Отсутствие электрического заряда у нейтрона затрудняет не только его обнаружение, но и управление им. Заряженные частицы могут быть ускорены, замедлены или отклонены электрическим или магнитным полями; на нейтроны же последние совершенно не действуют. Свободные нейтроны могут быть получены только в результате распада атомных ядер; естественного источника их нет. Единственный способ управления свободными нейтронами поставить на их пути ядра, которые будут их замедлять и отклонять или поглощать при столкновениях. Как мы увидим, эти явления имеют величайшее практическое значение.
ПОЗИТРОН И ДЕЙТРОН
1.21. В 1932 г. был открыт не только нейтрон, но также и позитрон. Позитрон впервые наблюдался К. Д. Андерсоном в Технологическом институте в Калифорнии. Масса его равна массе электрона, заряд по абсолютной величине такой же, как и у электрона, но имеет положительный знак.
Позитрон для нас интересен лишь как частица, испускаемая искусственными радиоактивными ядрами.
1.22. 1932 год был отмечен также другим важным открытием. Г. К. Юри, Ф. Г. Брикуэдде и Дж. М. Мерфи обнаружили у водорода изотоп с массовым числом 2, содержащийся в естественном водороде в количестве 1:5000. Благодаря особому значению этого тяжелого изотопа водорода, ему дали специальное название «дейтерий», а соответствующее ядро назвали дейтроном. Подобно ?-частице, дейтрон не является одной из основных частиц, но он играет важную роль в некоторых процессах, вызывающих распад ядра.
СТРОЕНИЕ ЯДРА
1.23. Все элементы состоят из нескольких основных частиц мысль уже не новая. Теперь это твердо установлено. Мы считаем, что существуют три основные частицы нейтрон, протон и электрон.
В фундаментальных работах обычно рассматривают еще позитрон, о котором мы уже упоминали, нейтрино и мезотрон. Дейтрон и ?-частица о них мы уже тоже говорили являются сложными частицами, играющими важную роль.
1.24. Согласно нашим современным взглядам, ядра всех атомов состоят из нейтронов и протонов. Число протонов равно атомному номеру Z. Число нейтронов, N, равно разности между массовым числом и атомным номером, т. е. А-Z.
Существуют два вида сил, действующих на эти частицы: обычные кулоновские силы электрического отталкивания между положительными зарядами и силы притяжения между всеми частицами, действующие на очень малых расстояниях. Последние силы не вполне изучены, и мы не будем пытаться рассматривать их. Достаточно сказать, что результирующее действие этих сил притяжения и отталкивания таково, что устойчивы только некоторые комбинации нейтронов и протонов. Если число нейтронов и протонов невелико, то комбинация устойчива, когда их количества примерно равны. Для больших ядер относительное число нейтронов. необходимых для устойчивости, больше. Наконец, в конце периодической таблицы, где число протонов свыше 90 и число нейтронов около 150, не существует вполне устойчивых ядер. (Некоторые из тяжелых ядер почти устойчивы, что подтверждается их очень большими периодами полураспада). Если искусственно образовать неустойчивое ядро путем добавления лишнего нейтрона или протона, то, в конце концов, происходит превращение, приводящее к устойчивому ядру. Как ни странно, это превращение сопровождается выбрасыванием не протона или нейтрона, а позитрона или электрона; по-видимому, внутри ядра протон превращается в нейтрон и позитрон (или нейтрон превращается в протон и электрон), а легкая заряженная частица выбрасывается. Другими словами, массовое число остается тем же самым, но атомный номер меняется. Условия устойчивости не очень строги, так что для данного массового числа, т. е. для данного общего числа протонов и нейтронов, может существовать несколько устойчивых расположений протонов и нейтронов (максимум три или пять), дающих несколько изобар. Для данного атомного номера, т. е. для данного числа протонов, условия могут варьироваться в еще более широких пределах, так что некоторые из тяжелых элементов имеют десять или двенадцать устойчивых изотопов. Известно около двухсот пятидесяти различных устойчивых ядер, для которых массовое число колеблется от единицы до двухсот тридцати восьми, а атомный номер от единицы до девяносто двух.
1.25. Все высказанные нами утверждения основаны на экспериментальных данных. Теория ядерных сил пока не завершена, но на основе принципов квантовой механики она была развита настолько, чтобы с ее помощью можно было объяснить не только описанные выше наблюдения, но и более подробные эмпирические данные об искусственной радиоактивности и о различиях между ядрами с четными и нечетными массовыми числами.
ИСКУССТВЕННАЯ РАДИОАКТИВНОСТЬ
1.26. Выше мы упоминали об испускании позитронов или электронов ядрами, стремящимися к устойчивости. Испускание электронов (?-лучей) уже было известно из изучения естественных радиоактивных веществ, но испускания позитронов для таких веществ обнаружено не было. В действительности, общие рассуждения, изложенные выше, были основаны частично на данных, которые выходят за рамки настоящего отчета. Однако, мы дадим краткое описание открытия «искусственной» радиоактивности и того, что мы о ней знаем.
1.27. В 1934 г. Кюри и Жолио сообщили о том, что некоторые легкие элементы (бор, магний, алюминий), подвергнутые бомбардировке ?-частицами, в течение известного времени продолжали испускать позитроны после того, как бомбардировка была прекращена. Другими словами, в результате бомбардировки ?-частицами бор, магний и алюминий становились радиоактивными. Кюри и Жолио измерили периоды полураспада радиоактивных веществ, образовавшихся под действием ?-частиц; они оказались равными 14 минутам, 2,5 минутам и 3,25 минутам соответственно.
1.28. Результаты, полученные Кюри и Жолио, послужили стимулом для проведения подобных опытов во всем мире. В частности, Э. Ферми пришел к выводу, что нейтроны, благодаря отсутствию у них заряда, должны, сравнительно легко проникать и внутрь тех ядер, которые имеют высокие атомные номера и в сильной степени отталкивают протоны и ?-частицы. Свое предположение он смог почти сразу подтвердить, обнаружив, что ядро атома, подвергшегося бомбардировке, захватывало нейтрон и что таким образом получалось неустойчивое ядро, которое затем приходило в устойчивое состояние путем испускания электрона. Следовательно, конечное устойчивое ядро имело массовое число на единицу выше, а также атомный номер на единицу выше, чем первоначальное ядро-мишень.
1.29. В результате множества опытов, проведенных с 1934 г. мы можем теперь получать радиоактивные изотопы почти каждого элемента периодической таблицы. Некоторые из них возвращаются к устойчивому состоянию испусканием позитронов, некоторые испусканием электронов, некоторые при помощи процесса, известного под названием захвата K-электрона, которого мы рассматривать не будем, и небольшое число ядер (вероятно три) становятся снова устойчивыми благодаря испусканию ?-частицы. Всего наблюдалось примерно пятьсот неустойчивых ядерных видов, и в большинстве случаев их атомные номера и массовые числа были установлены.
1.30. Искусственные радиоактивные элементы играют важную роль не только в осуществлении всего проекта, в котором мы заинтересованы, их будущее значение в медицине, в химии «меченых атомов» и во многих других областях научно-исследовательской работы вряд ли можно переоценить.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Мысли Менделеева о структуре атома
1869 год. 6 марта «Менделеев... совершил научный подвиг, который смело можно поставить рядом с открытием Леверье, вычислившего орбиту еще неизвестной планеты — Нептун».Ф. ЭНГЕЛЬС Был или не был порядок? о второй половине прошлого века наука какому пила уже довольно много
Глава 3. Строение атома
Глава 3. Строение атома Радиоактивность Блестящая серия физических открытий в последнее десятилетие XIX века поистине явилась началом научной революции. Прологом к ней послужило открытие, сделанное в 1896 году французским физиком Антуаном Анри Беккерелем, который
Радиоактивность
Радиоактивность Блестящая серия физических открытий в последнее десятилетие XIX века поистине явилась началом научной революции. Прологом к ней послужило открытие, сделанное в 1896 году французским физиком Антуаном Анри Беккерелем, который обнаружил, что соединения,
Строение ядра
Строение ядра Хотя вопрос об излучении ?-частицы казался окончательно выясненным, поскольку закон сохранения электрического заряда выполнялся, физики продолжали свои исследования. Для них оставалось загадкой, как положительно заряженное ядро способно испускать
Модели атома до Бора
Модели атома до Бора Развитие исследований радиоактивного излучения, с одной стороны, и квантовой теории — с другой, привели к созданию квантовой модели атома Резерфорда — Бора. Но созданию этой модели предшествовали попытки построить модель атома на основе
Искусственная радиоактивность
Искусственная радиоактивность Новый период в развитии ядерной физики начался фундаментальными открытиями. 15 января 1934 г. на заседании Парижской Академии наук Фредерик Жолио и Ирен Кюри сообщили об открытии ими нового вида радиоактивности. «Нам удалось доказать методом
Какова структура атома
Какова структура атома Модель атома водорода В 1913 году датский физик Нильс Бор (1885—1962) попытался нарисовать наглядную картину: как может быть построен атом из положительного ядра и электронов и при каких условиях он излучает свет. Физики называют такую наглядную
Модель атома водорода
Модель атома водорода В 1913 году датский физик Нильс Бор (1885—1962) попытался нарисовать наглядную картину: как может быть построен атом из положительного ядра и электронов и при каких условиях он излучает свет. Физики называют такую наглядную картину моделью атома.Задача
II. Строение атома
II. Строение атома Каждое химическое вещество состоит из однородных частиц, называемых молекулами. Если разложить молекулу на более элементарные составные части, мы получим атомы.Атом принято схематически изображать в виде ядра с вращающимися вокруг него электронами.
Глава 8. Внутри атома
Глава 8. Внутри атома Университетских студентов 1900 года учили тому, что обычное вещество — то, из которого состоят кирпичи, сталь, уран и все прочее, — и само состоит из мельчайших частиц, именуемых атомами. Однако, из чего состоят атомы, этого не знал никто. Общее мнение
X. Строение вещества
X. Строение вещества Молекулы Молекулы состоят из атомов. Атомы связаны в молекулы силами, которые называют химическими силами.Существуют молекулы, состоящие из двух, трех, четырех атомов. Крупнейшие молекулы – молекулы белков – состоят из десятков и даже сотен тысяч
Строение кристаллов
Строение кристаллов Почему так красива, правильна форма кристалла? Грани его, блестящие и ровные, выглядят так, словно над ними поработал искусный шлифовальщик. Отдельные части кристалла повторяют одна другую, образуя красивую симметричную фигуру.Ответ на поставленный
4.2. Физические характеристики, строение ядра
4.2. Физические характеристики, строение ядра В последнее десятилетие наши знания о кометах и о процессах, происходящих на них, значительно расширились. Резкому повышению интереса к кометам способствовали подготовка и проведение международного космического
Первая модель атома
Первая модель атома В заключение, мы можем сказать, что в первые годы XX в. был дан первый, может быть не полный, ответ на вопрос как излучается свет, а атомы с их электрическими зарядами были сочтены ответственными за это. Однако, как устроены атомы и, соответственно, каковы
БЕККЕРЕЛЬ И РАДИОАКТИВНОСТЬ
БЕККЕРЕЛЬ И РАДИОАКТИВНОСТЬ Анри Беккерель официально считается первооткрывателем радиоактивности, хотя он даже не дал ей названия — это сделала Мария — и на самом деле не открывал ее, поскольку это явление уже было обнаружено за несколько лет до него Ньепсом де