§ 50. Спектр атома водорода
Для полноты картины рассмотрим спектральную серию III. Чтобы узнать, куда попадают линии этой серии, вычислим для них наибольшую частоту. Она получается из (49.2) при n = 3 и m = ?. Тогда имеем: ??3 =3.29*1015/9 = 0.363х1015 (Гц). Это соответствует классической длине волны (? = c/?): ??3 = 2.99х108/0.363х1015 = 824 (нм). Известно, что видимый свет занимает диапазон примерно от 400 до 800 (нм). Следовательно, все линии серии III находятся в инфракрасной области, т. е. они невидимы. Серия № 3 носит имя Пашена. Имея инфракрасный спектрометр, можно выявить в этой области также серию Брэкета (n=4), Пфунда (n=5) и другие, представляющие скорее теоретический интерес. Таким образом, из всего спектра атома водорода человек может видеть только несколько фотонов из серии Бальмера (n = 2).
Полученные результаты будут более наглядны, если линии спектра водорода свести в таблицу. Во избежание путаницы, номера энергетических уровней (n, m) в атоме водорода взяты в круглые скобки. Значения энергии квантов поглощения, образующих серии (числа без скобок), посчитаны до серии № 6 (серия Хэмфри).
Таблица 1. Спектр поглощения атома водорода
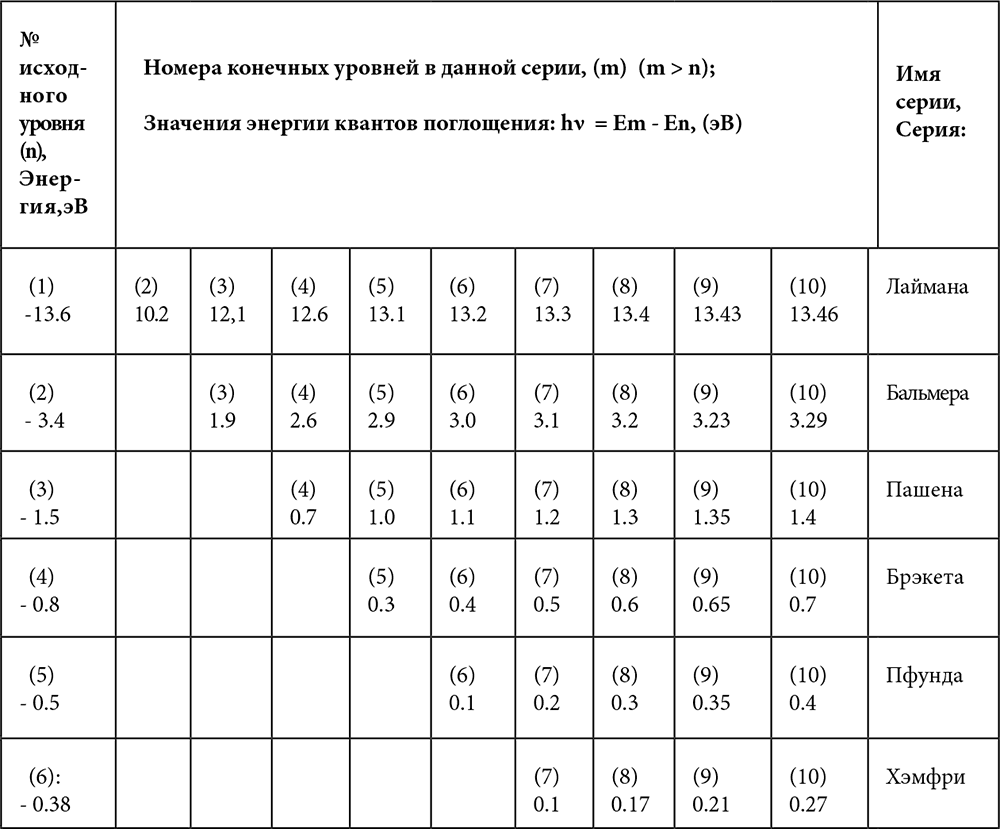
Задача. Предлагается рассчитать по формуле (49.2) серию линий для n=8 (вдруг серию № 7 уже кто-то посчитал). Получится серия № 8, которая будет лежать в очень далекой инфракрасной области (энергия квантов будет составлять сотые доли эВ). Эту серию читатель может назвать своим именем.
Следует заметить, что не все линии поглощения, указанные в таблице 1, можно увидеть даже при помощи спектрометра. Многое зависит от интенсивности – вероятности перехода электрона между конкретными орбитами. Если вероятность перехода мала, например, один-два в месяц, то это слишком мало, чтобы получилась четкая линия Фраунгофера.
Докажем, что теория квантов подтверждается спектральными данными, конкретно, значением постоянной Ридберга. Для этого умножим обе части уравнения (49.2) на h: h? = hR(1/n2 – 1/m2) = hR/n2 – hR/m2 (50.1). Из теории квантов: h? = Em – En (50.2). Подставив (50.2) в (50.1), получаем: Em – En = hR/n2 – hR/m2 (50.3). Уравнение (50.3) будет верно, если Em = – hR/m2 (50.4), и En = – hR/n2 (50.5). Уравнение (50.5) показывает, что энергия электрона зависит от обратного квадрата номера его орбиты. Подставляя R в (50.5), получаем для первой орбиты (n=1): Е1=-4.136*10-15*3.29*1015 = – 13.6 (эВ), что прекрасно совпадает с опытными данными (47.1). Если пойти дальше, то для n = 2: E2 = E1/4 = -13.6/4 = -3.4 (эВ), для № 3: E3 = -13.6/9 = -1.5, что полностью соответствует (47.1).
Мы доказали, что теория квантов объясняет линейчатость атомных спектров. Классическая теория МаксвеллаГерца не смогла это сделать.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК