Неподелённые пары тоже имеют значение
В главе 11 мы узнали, что для получения замкнутой электронной конфигурации атом C нуждается в образовании четырёх связей, для атома N требуется три связи, а для атома O — две связи. Если это будут связи с водородом, то получится метан, аммиак и вода: CH4, NH3 и H2O. При обсуждении молекулы HF в конце главы 13 мы отметили, что некоторые электроны атома F совершенно не были вовлечены в образование связей. Эти электроны находятся в спаренном состоянии, по сути, на атомных орбиталях, и называются неподелёнными парами. Неподелённые пары — это пары несвязывающих электронов, которые вызывают повышение электронной плотности в той области пространства, которую они занимают. Электроны, образующие связи, избегают располагаться вблизи неподелённых пар. Поэтому хотя неподелённые пары не являются связями, они также влияют на форму молекул. В связях электроны используются совместно и в основном концентрируются где-то между двумя атомами. Неподелённые пары не тянутся ко второму атому. Как следствие, их электронные облака расположены вблизи атомов, которым они принадлежат, и по размерам они больше, чем облака пар, образующих связи.
На рис. 14.2 изображены модели молекул метана, аммиака и воды. У аммиака имеется одна неподелённая пара, а у воды — две. Если принять в расчёт неподелённые пары, то все три молекулы имеют в своей основе тетраэдрическую форму. Однако аммиак и вода представляют собой неправильные тетраэдры. Неподелённая пара аммиака больше по размеру, чем связывающие пары. Чтобы минимизировать общее электрон-электронное отталкивание и достичь наименьшей энергии, связи удаляются от неподелённых пар, а значит, сближаются между собой. Угол HNH в молекуле аммиака составляет 107,3° — чуть меньше, чем в правильном тетраэдре. У воды две неподелённые пары, и поэтому угол между водород-кислородными связями уменьшается ещё сильнее — до 104,5°.
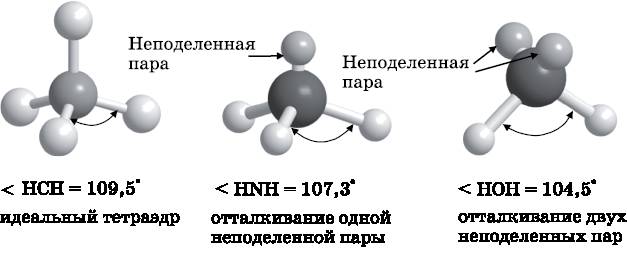
Рис. 14.2. Метан (слева), аммиак (посередине) и вода (справа). Неподелённые пары электронов отталкивают связывающие пары электронов, заставляя связи сближаться, из-за чего уменьшаются углы между связями атомов H с центральным атомом
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК