Делокализация пи-связей
На рис. 18.3 схематически изображены атомные орбитали, участвующие в образовании молекулярных орбиталей бензола. Сверху нарисованы гибридные атомные орбитали, служащие для создания ?-связей. Каждый атом углерода использует три гибридные sp2-орбитали для образования трёх ?-связей — одной с атомом водорода и по одной для двух соседних атомов углерода. Образование этих трёх sp2-гибридизированных атомных орбиталей оставляет каждому атому углерода по одной избыточной p-орбитали. В верхней части рис. 18.3 за плоскость xy принята плоскость, содержащая атомы (плоскость страницы). Тогда у каждого атома углерода остаётся неиспользованная pz-орбиталь, расположенная перпендикулярно плоскости страницы. Эти орбитали изображены в нижней части рисунка. Положительные и отрицательные лепестки орбиталей расположены над и под плоскостью кольца. На этой диаграмме длина связи между атомами углерода преувеличена, а ширина pz-орбиталей приуменьшена, чтобы сделать изображение более понятным. В действительности же pz-обитали перекрываются, что в более реалистичных пропорциях показано на рис. 14.15.
Эти шесть атомных pz-орбиталей объединяются и образуют молекулярные орбитали. Без нарушения принципа Паули эти атомные орбитали могут содержать максимум 12 электронов. Поэтому шесть атомных орбиталей образуют суперпозицию и дают шесть молекулярных орбиталей (МО), которые также могут вмещать максимум 12 электронов. Эти МО не связаны с конкретным атомом или даже конкретной парой атомов. Они растянуты на всю систему из шести атомов углерода.
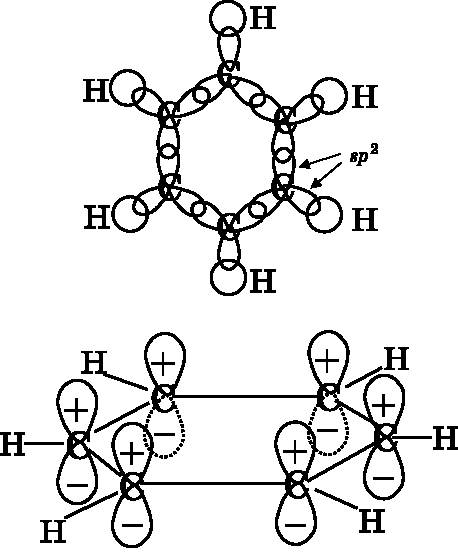
Рис. 18.3.Вверху: бензол и ?-связи. Каждый атом углерода образует три связи, используя три sp2-орбитали, лежащие в плоскости xy. У каждого атома углерода остаётся pz-орбиталь, перпендикулярная плоскости бензольного кольца. Внизу: pz-орбитали углерода имеют положительные и отрицательные лепестки, которые расположены над и под плоскостью кольца. Длина связей здесь преувеличена, а ширина лепестков, наоборот, приуменьшена для того, чтобы иллюстрация стала понятнее. Лепестки соседних pz-орбиталей перекрываются
Обсуждая молекулу водорода в связи с рис. 12.6, мы выяснили, что две атомные орбитали в ней объединяются и образуют две молекулярные орбитали — связывающую и разрыхляющую. В главе 13 мы разбирались с более крупными двухатомными молекулами, такими как F2, O2 и N2. У этих элементов каждый атом имеет три p-орбитали, а шесть атомных орбиталей при объединении дают шесть ?-МО — три связывающие и три разрыхляющие (см. рис. 13.5). Некоторые из этих двухатомных ?-МО будут вырожденными, то есть обладающими одинаковой энергией.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК