10. Альдегиды и кетоны
Альдегидами называются соединения, в которых карбонильная группа
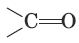
соединена с углеводородным радикалом и атомом водорода, а кетонами – карбонильные соединения с двумя углеводородными радикалами.
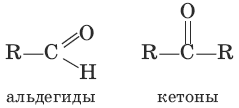
Систематические названия альдегидов строят по названию соответствующего углеводорода с добавлением суффикса –аль. Нумерацию цепи начинают с карбонильного атома углерода. Тривиальные названия производят от тривиальных названий тех кислот, в которые альдегиды превращаются при окислении: Н2С=O – метаналь (муравьиный альдегид, формальдегид); CH3CH=O – этаналь (уксусный альдегид). Систематические названия кетонов несложного строения производят от названий радикалов с добавлением слова «кетон». В более общем случае название кетона строится по названию соответствующего углеводорода и суффикса –он; нумерацию цепи начинают от конца цепи, ближайшего к карбонильной группе. Примеры: CH3—CO—CH3 – диметилкетон (пропанон, ацетон). Для альдегидов и кетонов характерна структурная изомерия. Изомерия альдегидов: а) изомерия углеродного скелета, начиная с С4; б) межклассовая изомерия. Изомерия кетонов: а) углеродного скелета (с С5); б) положения карбонильной группы (с С5); в) межклассовая изомерия.
Атомы углерода и кислорода в карбонильной группе находятся в состоянии sp2-гибридизации. Связь С=O сильно полярна. Электроны кратной связи С=O смещены к электроотрицательному атому кислорода, что приводит к появлению на нем частичного отрицательного заряда, а карбонильный атом углерода приобретает частичный положительный заряд.
Способы получения альдегидов и кетонов
1. а) (дегидрирование, окисление первичных спиртов)
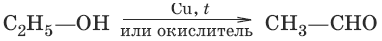
б) (дегидрирование, окисление вторичных спиртов)
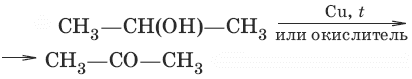
2. а) CH3CH2CHCl2 + 2NaOH ?в воде? CH3CH2CHO + 2NaCl + H2O (гидролиз дигалогенопроизводных)
б) CH3СCl2CH3 + 2NaOH ?в воде? CH3COCH3 + 2NaCl + H2O
3. (гидратация алкинов, реакция Кучерова)
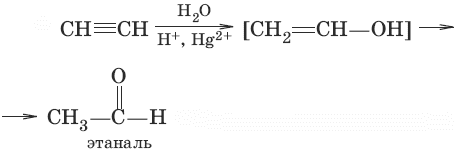
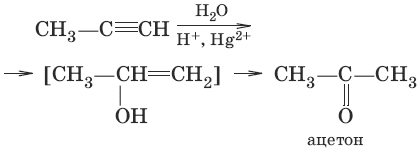
4. (окисление этилена до этаналя)
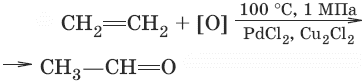
(окисление метана до формальдегида)
CH4 + O2 ?400–600 °C, NO? H2C=O + H2O
Химические свойства альдегидов и ке-тонов
Для карбонильных соединений характерны реакции различных типов: а) присоединение по карбонильной группе; б) восстановление и окисление; в) конденсация; д) полимеризация.
1. (присоединение циановодородной кислоты, образование гидроксинитрилов)
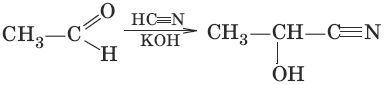
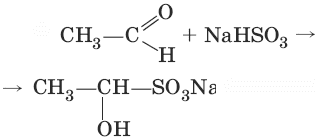
2. (присоединение гидросулбфита натрия)
3. (восстановление)
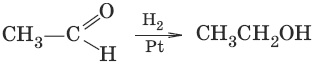
4. (образование полуацеталец и ацеталей)
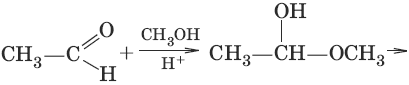
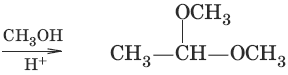
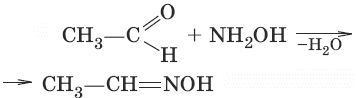
5. (взаимодействие с гидроксоламином, образование оксима ацетальдегида)
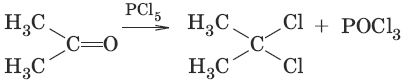
6. (образование дигалогенопроизводных)
7. (?-галогенирование в присутствии OH?)
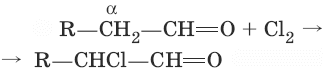
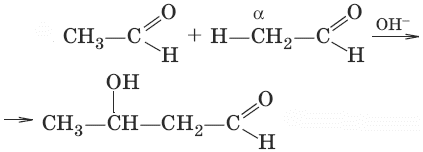
8. (албдольная конденсация)
9. R—CH=O + Ag2O ?NH3? R—COOH + 2Ag? (окисление, реакция «серебряного зеркала»)
R—CH=O + 2Cu(OH)2 ? R—COOH + Cu2O?, + 2H2O (красный осадок, окисление)
10. (окисление кетонов, жесткие условия)
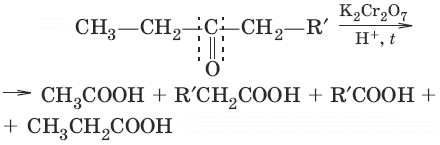
11. nCH2=O ? (—CH2—O—)n параформ n = 8—12 (полимеризация)
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК