Тройная точка
Тройная точка
Итак, имеются условия, при которых пар, жидкость и кристалл могут попарно существовать в равновесии.
Могут ли находиться в равновесии все состояния? Такая точка на диаграмме давление – температура существует, ее называют тройной. Где она находится?
Если поместить в закрытый сосуд при нуле градусов воду с плавающим льдом, то в свободное пространство начнут поступать водяные (и «ледяные») пары. При давлении 4,6 мм Нg испарение прекратится, и начнется насыщение. Теперь три фазы – лед, вода и пар – будут в состоянии равновесия. Это и есть тройная точка.
Соотношения между различными состояниями наглядно и отчетливо показывает диаграмма для воды, изображенная на рис. 103.
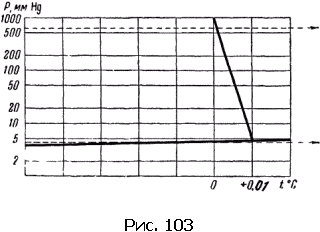
Такую диаграмму можно построить для любого тела.
Кривые на рисунке нам знакомы – это кривые равновесия между льдом и паром, льдом и водой, водой и паром. По вертикали, как обычно, откладывается давление, по горизонтали – температура.
Три кривые пересекаются в тройной точке и делят диаграмму на три области – жизненные пространства льда, воды и водяного пара.
Диаграмма состояния – это сжатый справочник. Ее цель – дать ответ на вопрос, какое состояние тела устойчиво при таком-то давлении и такой-то температуре.
Если в условия «левой области» поместить воду или пар, то они станут льдом. Если в «нижнюю область» внести жидкость или твердое тело, то получится пар. В «правой области» пар будет конденсироваться, а лед плавиться.
Диаграмма существования фаз позволяет сразу же ответить, что произойдет с веществом при нагревании или при сжатии. Нагревание при неизменном давлении изобразится на диаграмме горизонтальной линией. Вдоль этой линии слева направо движется точка, изображающая состояние тела.
На рисунке изображены две такие линии, одна из них – это нагревание при нормальном давлении. Линия лежит выше тройной точки. Поэтому она пересечет сначала кривую плавления, а затем, за пределами чертежа, и кривую испарения. Лед при нормальном давлении расплавится при температуре 0 °C, а образовавшаяся вода закипит при 100 °C.
Иначе будет обстоять дело для льда, нагреваемого при очень небольшом давлении, скажем, чуть ниже 5 мм Hg.
Процесс нагревания изобразится линией, идущей ниже тройной точки. Кривые плавления и кипения не пересекаются этой линией. При таком незначительном давлении нагревание приведет к непосредственному переходу льда в пар.
На рис. 104 эта же диаграмма показывает, какое интересное явление произойдет при сжатии водяного пара в состоянии, помеченном на рисунке крестиком. Сначала пар превратится в лед, а затем расплавится. Рисунок позволяет тут же сказать, при каком давлении начнется рост кристалла и когда произойдет плавление.
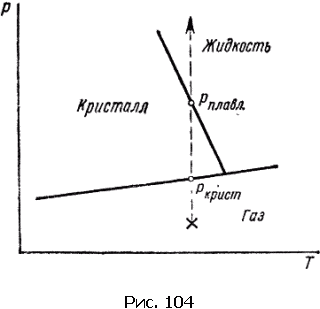
Диаграммы состояния всех веществ похожи одна на другую. Большие, с житейской точки зрения, различия возникают из-за того, что место нахождения тройной точки на диаграмме может быть у разных веществ самым различным.
Ведь мы существуем вблизи «нормальных условий», т.е. прежде всего при давлении, близком к одной атмосфере. Как расположена тройная точка вещества по отношению к линии нормального давления – для нас очень существенно.
Если давление в тройной точке меньше атмосферного, то для нас, живущих в «нормальных» условиях, вещество относится к плавящимся. При повышении температуры оно сначала превращается в жидкость, а потом закипает. В обратном случае – когда давление в тройной точке выше атмосферного – мы при нагревании не увидим жидкости, твердое вещество будет прямо превращаться в пар. Так ведет себя «сухой лед», что очень удобно для продавцов мороженого. Брикеты мороженого можно перекладывать кусками «сухого льда» и не бояться при этом, что мороженое станет мокрым. «Сухой лед» – это твердый углекислый газ CO2. Тройная точка этого вещества лежит при 73 атм. Поэтому при нагревании твердого СО2 точка, изображающая его состояние, движется по горизонтали, пересекающей только лишь кривую испарения твердого тела (так же, как и для обычного льда при давлении около 5 мм Нg).
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Точка опоры
Точка опоры «Дайте мне точку опоры, и я переверну мир!» Кто это хвастался? Вы, конечно, знаете — Архимед. Мир он не перевернул, но мысль была правильной. Во всяком революционном перевороте нужна надежная основа, на которую можно с уверенностью опереться. Так и философам
90 Точка концентрации напряжений, или Как остановить трещину на стекле
90 Точка концентрации напряжений, или Как остановить трещину на стекле Для опыта нам потребуются: две длинные палки. Ну, раз уж начали про стекло, давайте подумаем над занятным вопросом. Часто бывает, что по стеклу начинает бежать трещина. Чаще всего это заметно на лобовых
Точка зрения звездного наблюдателя
Точка зрения звездного наблюдателя Мы решили изучать движение с точки зрения инерциальных систем. Не придется ли тогда отказаться от услуг земного наблюдателя? Ведь Земля вращается вокруг оси и вокруг Солнца, как доказал Коперник. Сейчас читателю, может быть, трудно
МЕРТВАЯ ТОЧКА
МЕРТВАЯ ТОЧКА Казалось, что Фарадею предназначено судьбой стать революционером в области электромагнетизма. Ему даже удалось избавиться от ограничений брака и полностью посвятить себя науке, но на пути ученого возникло новое препятствие. Разочарование пришло со
Точка – линия – квадрат – куб – тессеракт
Точка – линия – квадрат – куб – тессеракт Обычный тессеракт – это гиперкуб, куб в четырех измерениях. С помощью рис. 29.1 и 29.2 я по шагам объясню, что это значит. Если мы возьмем точку (рис. 29.1 сверху) и будем двигать ее в одном измерении, мы получим линию (точнее